Электроаналитические методы
![]()
В аналитической практике электрогравиметрические определения проводят при плотности тока от 0,1 до 10 А/см2.
3. Перемешивание и температура раствора
Электрогравиметрические определения проводят обычно при механическом перемешивании раствора и температуре 50-60°С для уменьшения поляризационных явлений, концентрационной
и кинетической поляризации. Дальнейшее повышение температуры может привести к выпариванию раствора, повышению поляризации вещества и возникновению концентрационной поляризации.
4. рН раствора
Кислотность среды строго контролируется, поскольку кислое значение рН может вызвать образование газообразного водорода, что приводит к уменьшению выхода по току выделения металла и образованию рыхлых осадков.
5. Присутствие комплексообразователей
Экспериментально установлено, что выделение металлов из растворов их комплексных солей осуществляется при более отрицательных рН их потенциала, чем выделение из чистых металлов катионов. Возможность связывания некоторых катионов в комплексы позволяет повысить селективность выделения металла и соответственно точность их разделения.
Анодные осадки
Большинство катионов металлов способных давать удовлетворительные катодные осадки определяют путем восстановления на катоде. Исключение Pb2+, который определяют, окисляя на аноде од PbO2 в виде черного осадка на поверхности анода.
К числу электрогравиметрических определений относят использование в качестве анода серебряной проволоки и образования малорастворимых соединений серебра в процессе его анодного растворения.
3.4 Кулонометрические определения
Кулонометрические определения проводят в том случае, когда и окисленная и восстановленная формы вещества присутствуют в растворенном виде.
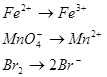
В кулонометрии используют второй закон Фарадея: при пропускании через раствор одного и того же количества электричества на электродах превращаются эквивалентные количества вещества. Обязательным условием проведения кулонометрических определений является использование реакций со 100% выходом по току.
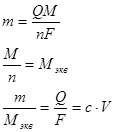
В кулонометрии очень часто возникает необходимость дополнительного определения количества образующегося продукта реакции или установления количества прореагировавшего исходного вещества. В этом случае используют либо потенциометрические, либо титриметрические методы анализа.
Так же как и гравиметрические методы, кулонометрические определения можно проводить при постоянном потенциале электрода, либо при постоянной силе тока.
Кулонометрия при постоянной силе тока может привести к потере селективности определения, если не поддерживать силу тока путем постоянного увеличения наложенного напряжения. Гораздо чаще в современной аналитической практике используют кулонометрию при постоянном потенциале электрода.
При постоянном потенциале электрода обеспечивается количественное окисление или восстановление вещества при этом на рабочем электроде не должны претерпевать превращения сторонние вещества. То есть выход по току должен составлять 100%. Количество электричества необходимое для превращения определяемого вещества определяют с помощью кулонометра. При этом определяемое вещество не всегда может принимать участие в электродной реакции. Например, определение анионов на серебряном аноде.
Кулонометрия при постоянном контролируемом потенциале катода обладает всеми преимуществами метода и лишена недостатков электрогравиметрического определения при контролируемом потенциале катода. Кулонометрически можно определять те катионы металлов, которые не образуют удовлетворительных по качеству осадков на катоде. Для поддержания потенциала рабочего электрода используют потенциостат, то есть трехэлектродную ячейку.
3.5 Кулонометрическое титрование
Суть метода: через анализируемый раствор пропускают постоянный ток до тех пор, пока индикатор не укажет на завершение реакции количество затраченного электричества определяемого как произведение постоянной силы тока на время, в течение которого ток пропускают через раствор. Именно поэтому за время кулонометрического титрования необходимо поддерживать силу тока постоянной. Поскольку возникающая концентрационная поляризация приводит к увеличению потенциала рабочего электрода. Очень часто титрант генерируется на одном из электродов, который называют генератором.
Количество генерируемого титранта контролируется количеством электричества пропущенного через раствор.
Преимущества кулонометрического титрования
1. Отсутствие проблем связанных с приготовлением, хранением и стандартизацией рабочих растворов.
2. Возможность генерации малых количеств титранта путем регулирования силы тока
3. Один и тот же источник постоянного тока может быть использован для генерации титрантов в нескольких ячейках подключенных последовательно.
Возможные ошибки метода
1. Существенное значение силы тока от заданного значения
2. Отклонение выхода по току от 100%
3. Ошибки в измерении силы тока
4. Ошибки в измерении времени
5. Индикаторные ошибки, связанные с определением конечной точки титрования
В кулонометрическом титровании можно использовать все виды реакций между определяемым веществом и титрантом.
1. Кислотно-основное титрование. С достаточно высокой точностью титруются и слабые и сильные кислоты электрогенерированными ОН--ионами на платиновом аноде. При этом необходимо использовать полупроницаемую мембрану, чтоб отделить поле анода от ионов водорода из анализируемого раствора.
2. Окислительно-восстановительное титрование применяется в кулонометрии, поскольку большое количество окислителей и восстановителей способны образовываться на генераторном электроде.
3. Комплексонометрическое титрование. Кулонометрический метод применяют для титрования двух- или трехзарядных катионов металлов ионами НY3- генерированными на ртутном катоде. Для генерации используют комплексонат ртути (ІІ) в аммиачной среде
![]()
Таким образом, используют кулонометрическое комплексонометрическое титрование
4. Осадительное титрование. В качестве генератора используют инертный анод, образующиеся ионы Ag+ связывают присутствующие в анализируемом растворе галогенид-анионы S2-, SCN-, CrO42- и т.д.
3.6 Общая характеристика метода
Кулонометрический метод позволяет определять очень небольшое содержание вещества с высокой точностью (0,1…0,05%), превосходя в этом отношении многие другие методы. Кулонометрия характеризуется также высокой селективностью (избирательностью), позволяя определять многие вещества в растворе без предварительного химического разделения. Избирательность обеспечивается обоснованным выбором рабочего потенциала электрода и поддерживанием его постоянного значения с высокой точностью во все время электролиза. Кулонометрический анализ не требует какой-либо предварительной градуировки измерительных приборов по концентрации или построения градуировочных графиков, связывающих свойство вещества с его концентрацией, и в этом смысле кулонометрию следует считать абсолютным методом.
