Электроаналитические методы
Химические сенсоры
Необходимость постоянного мониторинга многих объектов требует наличие портативных, миниатюрных устройств и способных моментально выдавать информацию об анализируемом объекте.
Все сенсоры делят на две большие группы:
1. Физические сенсоры, реагирующие на такие факторы как температура, давление, магнитное поле и силы, не являющиеся предметом х
имии.
2. Химические сенсоры, реагирующие на специфические химические реакции, в том числе и биохимические. В общем случае химический сенсор – устройство, избирательно реагирующее на конкретный химический объект путем химической реакции, которую которое можно использовать для количественного или качественного определения аналита.
Любой химический сенсор состоит из двух компонентов:
1 – собственно блок, где происходит химическая реакция;
2 – преобразователь (трансдьюсер).
Химические сенсоры делят на ряд групп в зависимости от типа преобразователя.
1) Электрохимические сенсоры: потенциометрические, вольтамперометрические.
Потенциометрические сенсоры или ионоселективные полевые транзисторы используют метод прямой потенциометрии для проведения измерений.
Вольтамперометрические или амперометрические сенсоры используют зависимость силы тока от поданного на систему потенциала, для контроля содержания определяемого компонента.
2) Оптические сенсоры. Спектроскопическое определение в оптических сенсорах связано с химической реакцией. В настоящее время оптические сенсоры называю оптодатчиками. В зависимости от типов оптических сенсоров в них измеряют поглощение, отражение света или люминесценцию.
3) Массчувствительные
4) Теплочувствительные. Сенсоры, относящиеся к этой группе часто называют калориметрическими, так как они используют тепловой эффект химической реакции.
В отдельную группу часто выделяют биосенсоры, то есть устройства позволяющие контролировать биологически активные компоненты на основе высокоселективных биохимических реакций. В этом виде сенсоров чаще всего применяют электрохимические и оптические трансдьюсеры.
1.5 Потенциометрическое титрование
Потенциометрическое титрование используют в тех случаях, когда применение цветных индикаторов не возможно: титрование сильно окрашенных, мутных растворах и смесей. В случае потенциометрического титрования важным является выбор индикаторного электрода. При кислотно-основном титровании используется стеклянный рН-чувствительный электрод. При осадительном титровании используют металлические электроды первого или второго рода. При титровании органических соединений методом осаждения используют ИСЭ. При окислительно-восстановительном титровании используют платиновый инертный окислительно-восстановительный электрод. В случае комплексонометрического титрования используют электроды второго и третьего рода.
Конечную точку титрования определяют по резкому изменению (скачку) потенциала.
Точка эквивалентности при потенциометрическом титровании определяется графически по одному из четырех графиков (рис. 1.3)
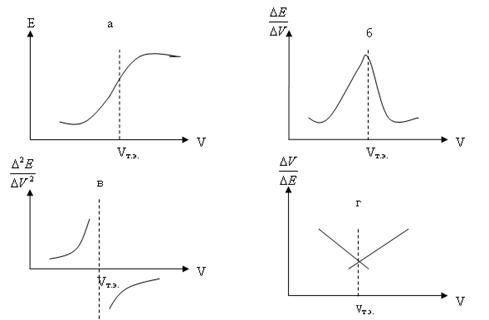
Рисунок 1.3 – Кривые потенциометрического титрования: а – обычная кривая; б – дифференциальная кривая; в – кривая титрования по второй производной; г – кривая Грана
1.6 Общая характеристика метода
Основными достоинствами потенциометрического метода являются его высокая точность, высокая чувствительность и возможность проводить титрования в более разбавленных растворах, чем это позволяют визуальные индикаторные методы. Необходимо отметить также возможности определения этим методом нескольких веществ в одном растворе без предварительного разделения и титрования в мутных и окрашенных средах. Значительно расширяется область практического применения потенциометрического титрования при использовании неводных растворителей. Они позволяют, например, найти содержание компонентов, которые в водном растворе раздельно не титруются, провести анализ веществ, нерастворимых или разлагающихся в воде и т.д. Немаловажным достоинством потенциометрии является также возможность автоматизировать процесс титрования.
К недостаткам потенциометрического титрования можно отнести не всегда быстрое установление потенциала после добавления титранта и необходимость во многих случаях делать при титровании большое число отсчетов.
2. Вольтамперометрия
Вольтамперометрия основана на изучении поляризационных или вольтамперных кривых (кривых зависимости силы тока I от напряжения Е), которые получают в процессе электролиза раствора анализируемого вещества при постепенном повышении напряжения с одновременной фиксацией при этом силы тока. Электролиз проводят с использованием легкополяризуемого электрода с небольшой поверхностью, на котором происходит электровосстановление или электроокисление вещества.
2.1 Полярография
Вольтамперометрию, связанную с использованием ртутного капающего электрода (РКЭ), называют полярографией. Характерной особенностью полярографического метода является применение электродов с разной площадью поверхности. Поверхность одного из электродов, называемого микроэлектродом, должна быть во много раз меньше поверхности другого электрода. В качестве микроэлектрода чаще всего применяют РКЭ, представляющий собой капилляр, из которого равномерно с определенной скоростью вытекают капли металлической ртути. Скорость прокапывания определяется высотой подвески емкости с ртутью, соединенной шлангом с капилляром. Второй электрод, поверхность которого во много раз больше поверхности микроэлектрода, служит электродом сравнения. В качестве него используют ртуть, налитую на дно электролитической ячейки, или насыщенный каломельный электрод. На эти электроды от внешнего источника напряжения подают плавно изменяющееся напряжение. Плотность тока (А/см2) на электроде сравнения, имеющего большую поверхность, ничтожно мала, поэтому потенциал его практически не изменяется, т.е. этот электрод не поляризуется. Плотность тока на РКЭ вследствие его малой поверхности высока. РКЭ изменяет свой равновесный потенциал, т.е. поляризуется. Реализацию метода осуществляют на приборах, называемых полярографами. Принципиальная схема полярографа приведена на рис. 2.1. Ток от аккумулятора поступает на реостат, при помощи которого через очень чувствительный гальванометр подается плавно повышающееся напряжение на электролитическую ячейку, содержащую ртутный (или каломельный) электрод, РКЭ и анализируемый раствор.
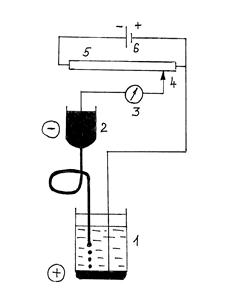
Рисунок 2.1 – Схема полярографической установки: 1 - электролизёр; 2 - сосуд с ртутью; 3 - гальванометр; 4 - передвижной контакт; 5 - реохорд; 6 - аккумулятор.
Вольтамперные кривые
Фиксируя силу тока, проходящего через ячейку, в зависимости от поданного напряжения, получают вольтамперные кривые, называемые в полярографии полярограммами (рис. 2.2). Форма полярограмм напоминает волну. Первый участок волны (АБ) соответствует начальному моменту процесса, когда протекает только остаточный (конденсаторный или емкостной) ток, связанный с расходом некоторого количества электричества на заряжение двойного электрического слоя на поверхности капли ртути и восстановлением следовых количеств электроактивных примесей.
