Электроаналитические методы
![]()
Потенциал ячейки будет определяться потенциалами двух электродов сравнения; потенциалом мембраны и еще одной величиной, которую называют потенциалом ассиметрии.
![]()
Потенциал ассиметрии возникает даже в случае, если мы используем совершенно идентичные вне
шние и внутренние электроды сравнения.
Появление этой величины связывают с различным диаметром внешней и внутренней поверхности шарика, что может привести к различным напряжениям в стеклянной матрице мембраны и соответственно к различной скорости обмена ионами водорода на внешней и внутренней поверхности мембраны.
По мере использования электрода наружная рабочая поверхность шарика загрязняется молекулами различных веществ, что приводит к повышению потенциала ассиметрии и соответственно погрешностям в измерении величины рН. Потому необходимо тщательно отмывать стеклянный электрод после погружения его в растворы сложного состава рН 5,5÷6,0.
Сам процесс обмена ионами водорода между раствором и стеклянной мембранной осуществляется в тонком гелевом слое, который образуется на обеих поверхностях мембраны при выдерживании электрода в дистиллированной воде.
При выдерживании стеклянного электрода в воде в гелевом слое образуются так называемые силанольные группы ![]() .
.
Если выдержать мембрану в растворе соляной кислоты определенной концентрации, ионы водорода, проникая в поры мембраны, образуют связь с неподеленной парой ![]() кислорода силанольной группы.
кислорода силанольной группы.
Наличие неподеленной пары ![]() для атома кислорода силанольной группы позволяет ионам водорода, протекающим извне образовывать связь –O:H+. Именно для того, чтобы мембрана стеклянного электрода насытилась ионами Н+, электрод вымачивают в течение нескольких дней в растворе 0,1М HCl и именно эти ионы участвуют потом в ионном обмене при опускании электрода в анализируемый раствор. В более старых теориях формирования потенциала рН-чувствительной мембраны оговаривалось, что ионы Н+ из анализируемого раствора эквивалентно обменивается с ионами щелочных металлов из матрицы мембраны.
для атома кислорода силанольной группы позволяет ионам водорода, протекающим извне образовывать связь –O:H+. Именно для того, чтобы мембрана стеклянного электрода насытилась ионами Н+, электрод вымачивают в течение нескольких дней в растворе 0,1М HCl и именно эти ионы участвуют потом в ионном обмене при опускании электрода в анализируемый раствор. В более старых теориях формирования потенциала рН-чувствительной мембраны оговаривалось, что ионы Н+ из анализируемого раствора эквивалентно обменивается с ионами щелочных металлов из матрицы мембраны.
Перечисленные теории объясняют физический смысл операций, которые необходимо проводить со стеклянным электродом для получения удовлетворительных и воспроизводимых результатов измерения.
1. «Вымачивание» нового электрода в 0,1М растворе HCl не менее трех дней.
2. Хранение рабочих электродов исключительно в Н2Одист рН 5,5÷6,0
В области сильнокислых (рН<1) и сильнощелочных (рН>12) растворов возможно появление ошибок в измерении величины рН. Так называемая щелочная ошибка (рН>12) связана с участием в формировании потенциала электрода ионов Na+ или К+, которые также способны участвовать в ионном обмене. Ошибки измерения рН в сильнокислой среде (рН<1) обусловлены тем, что теоретические расчеты рН сильнокислых растворов необходимо проводить с учетом функции Гамета, поскольку заметный избыток ионов Н+ в сильнокислом растворе требует использования дополнительных буферных растворов.
Б) Мембранные электроды с жидкими мембранами
Применение жидких мембран основано на том, что они обладают потенциалом, устанавливающемся на поверхности между анализируемым раствором и несмешивающейся жидкостью селективно реагирующей с анализируемым ионом. Электроды с жидкими мембранами позволяют проводить прямые потенциометрические определения некоторых многозарядных катионов, а также ряда анионов. Электрод с жидкой мембраной отличается от стеклянной мембраны только тем, что растворы с известной и неизвестной активностью анализируемого иона разделены не стеклянной мембраной, а тонким слоем несмешивающейся органической жидкости. Вариантом таких электродов являются электроды с пленочными мембранами. Мембрана такого электрода представляет собой – тонкую полимерную пленку, в которой равномерно распределяется ионообменник, то есть соединение, содержащее анализируемый ион.
В) Электроды с твердыми мембранами
Селективность стеклянной мембраны обусловлено наличием анионных пустот (например, пара ![]() у атома кислорода) обладающим определенным сродством к положительно заряженным ионам. Аналогично, можно сказать, что мембраны, имеющие катионные пустоты будут обладать селективностью к анионам. Были изготовлены мембраны в виде таблеток из кристаллов солей малорастворимых соединений. Чтобы изготовить такую твердую мембрану необходимо вырастить монокристалл соответствующей соли.
у атома кислорода) обладающим определенным сродством к положительно заряженным ионам. Аналогично, можно сказать, что мембраны, имеющие катионные пустоты будут обладать селективностью к анионам. Были изготовлены мембраны в виде таблеток из кристаллов солей малорастворимых соединений. Чтобы изготовить такую твердую мембрану необходимо вырастить монокристалл соответствующей соли.
Г) Электроды с газочувствительными мембранами
Газочувствительная мембрана представляет собой тонкую газопроникающую керамическую мембрану, которая разделяет внутренний раствор с известной активностью определяемого иона и внешний анализируемый раствор. Тонкие микропористые мембраны изготавливаю из гидрофобного пластика. Потенциал формируется за счет обмена молекулами газа между анализируемым раствором и мембраной. Применяют в анализе SO2, SO3, Cl2, NH3CO.
1.4 Прямая потенциометрия
Метод достаточно прост и состоит в сравнении потенциала индикаторного электрода в растворе определенного вещества с потенциалом его же электрода, погруженный в стандартный раствор его же вещества.
В аналитической практике для определения концентрации используют метод сравнения со стандартом, метод градировочного график, метод добавок.
Метод добавок позволяет анализировать достаточно разбавленные растворы, что заметно расширяет применимость прямой потенциометрии.
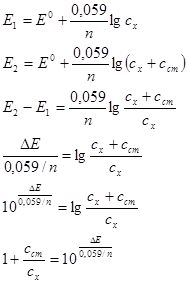
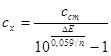
Ионометрия или прямая потенциометрия с применением ионоселективных электродов
Ионоселективным электродом (ИСЭ) называется электрохимический полуэлемент, в котором разность потенциалов на границе раздела фаз электродный материал – электролит зависит от концентрации (активности) определяемого иона в растворе. В большинстве своем ИСЭ это мембранные электроды.
Химико-аналитические характеристики ИСЭ
1. Электродная функция – зависимость потенциала ИСЭ от отрицательного логарифма концентрации стандартных растворов (рС).
Для построения графика электродной функции ИСЭ измеряют потенциал электрода в зависимости от концентрации стандартных растворов, которая отличается чаще всего на порядок: 10-1; 10-2; 10-3; 10-4; 10-5.
2. Крутизна электродной функции – тангенс угла наклона линейного участка электродной функции и оси х.
![]()
Точность определения с данным ИСЭ будет зависеть от того, насколько крутизна полученной электродной функции отличается от Нернстовской зависимости.
