Принципы биохимического исследования
рН = рКа ± 1
Буферы, применяемые для биологических исследований, должны удовлетворять ряду требований:
1. Обладать достаточной буферной емкостью в требуемом диапазоне значений рН.
2. Обладать высокой степенью чистоты.
3. Хорошо растворяться в воде и не проникать через биологические мембраны.
4. Обладать устойчивостью к действию ферментов и гидролизу.
5. рН буферных раств
оров должен как можно меньше зависеть от их концентрации, температуры и ионного или солевого состава среды.
6. Не оказывать токсического или ингибирующего действия.
7. Комплексы буфера с катионами должны быть растворимыми.
8. Не поглощать свет в видимой или ультрафиолетовой областях спектра.
К сожалению, этим требованиям удовлетворяют далеко не все буферные растворы. Так, фосфаты обладают способностью осаждать поливалентные катионы и во многих системах выступают в качестве метаболитов или ингибиторов; трис-буфер иногда оказывает токсическое или ингибирующее действие. До недавнего времени насчитывалось всего несколько буферов, рН которых лежит в важной для биохимии области 6,0—8,0 и которые удовлетворяют перечисленным выше требованиям. В последние годы, однако, появился целый ряд так называемых цвиттерионных буферов типа ГЭПЭС и ПИГТЭС. Некоторые наиболее распространенные буферы приведены в табл. 1.1. Для получения буферных растворов, применимых в широком диапазоне значений рН, используются смеси разных буферов. Например, буферы Мак-Ильвейна имеют рН с областью значений от 2,2 до 8,0 и приготавливаются из лимонной кислоты и двузамещенного фосфорнокислого натрия.
Наиболее важной группой физиологических буферов являются белки. Благодаря большому количеству содержащихся в боковых цепях аминокислот щелочных и слабокислых групп белки имеют очень высокую буферную емкость. Буферная емкость крови в основном определяется гемоглобином.
1.3 Зависимость ионизации аминокислот и белков от рН
Аминокислоты и белки — это наиболее важные в биологическом отношении соединения, поэтому необходимо знать, в какой степени изменение рН влияет на их физические свойства. За исключением пролина, химические формулы всех аминокислот, из которых синтезируются белки, можно записать в общем ' виде как RCH(NH2)COOH. рН аминогруппы лежит в области 9,0—10,5, а карбоксильной группы — между 1,7 и 2,4.
Степень ионизации аминокислот в водных растворах зависит от рН и определяется уравнением Гендерсона—Хассельбальха.
![]()
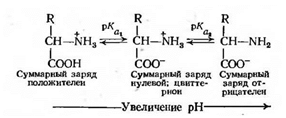 |
Таким образом, при низких значениях рН аминокислота находится в катионной форме, а при высоких — в анионной. При некотором промежуточном значении рН аминокислота оказывается незаряженной и называется цвиттерионом. Было установлено, что в кристаллическом состоянии или после растворения в чистой воде такие аминокислоты существуют главным образом в виде цвиттерионов, что придает им свойства ионных соединений, а именно высокую точку плавления и кипения, хорошую растворимость в воде и плохую растворимость в таких органических растворителях, как эфир и хлороформ. Величина рН, при которой в водном растворе преобладает цвиттерион, называется изоионной точкой: число отрицательных зарядов, образующихся на молекуле в результате отщепления протонов, равно числу положительных зарядов, образующихся благодаря присоединению протонов. Для аминокислот эта величина приблизительно соответствует изоэлектрической точке (pi) — молекула не несет суммарного заряда и таким образом оказывается электрофоретически неподвижной. Численное значение рН для этого случая зависит от того, насколько сильной является кислота, и определяется следующим уравнением:
Для глицина величины рКа, Н рКаг равны 2, 3 и 9,6 соответственно; следовательно, изоионная точка равна 6,0. При более низких значениях рН в растворе содержатся и цвиттерион, и катион, а соотношение между ними определяется уравнением Гендерсона — Хассельбальха; при более высоких рН наряду с цвиттерионом в растворе находится анион.
Для так называемых «кислых» аминокислот, например, аспарагиновой кислоты; ионизация носит несколько иной характер. Это обусловлено наличием у них второй карбоксильной группы.
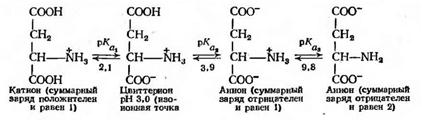
В этом случае рН, при котором в водном растворе преобладает цвиттерион, определяется величинами рСа, и рКаз
Для лизина, который является «основной» аминокислотой, изоионная точка определяется величинами рКа2 и рКа3- Ионизация происходит следующим образом:
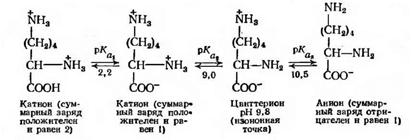
Вместо второй амино- или карбоксильной группы боковая цепь аминокислоты иногда содержит другую химическую группу, которая при определенном значении рН также ионизуется. К таким группам относятся фенольная (тирозин), гуанидиновая (аргинин), имидазольная (гистидин) и сульфгидрильная группа (цистеин). Ясно, что степень ионизации различных основных групп аминокислот при одном и том же рН будет различной. Более того, небольшие различия могут наблюдаться даже у одной и той же группы. Эти различия используют при электрофоретическом и ионообменном разделении смесей аминокислот, имеющихся, например, в белковом гидролизате.
Ионизация молекул белка качественно напоминает ионизацию аминокислот, но в количественном отношении отличается от нее благодаря наличию большого числа способных к ионизации групп. Белки образуются путем конденсации а-аминогруппы одной аминокислоты с о-карбоксильной группой соседней аминокислоты, поэтому, за исключением двух концевых аминокислот, все о амино- и карбоксильные группы участвуют в образовании пептидных связей и в белке не ионизуются. Однако в боковых цепях присутствуют сотни амино- и карбоксильных групп, которые могут легко ионизоваться. Электростатическое притяжение, возникающее между некоторыми из этих групп, способствует стабилизации третичной структуры белковой молекулы, при этом молекулы белков часто бывают свернуты таким образом, что большинство способных к ионизации групп оказываются расположенными на поверхности молекулы, где они могут вступать во взаимодействие с окружающей средой. Естественно, что относительное число положительно и отрицательно заряженных групп в молекуле белка определяет те или иные ее физические свойства. У гистонов преобладают катионные группы, в то время как в других белках количество анионных и катионных групп либо одинаково, либо, напротив, преобладают анионные группы.
В отличие от аминокислот у белков изоионная точка обычно не совпадает с изоэлектрической. По определению изоионная точка — это такая величина рН, при которой молекула белка содержит равное число положительно и отрицательно заряженных групп, образовавшихся в результате связывания основных групп с протонами и соответствующей диссоциации кислотных групп. Изоэлектрическая точка — это рН, при котором белок электрофоретически неподвижен. При ее определении белок растворяют в буферном растворе. В этом растворе всегда содержатся низкомолекулярные анионы и катионы, способные связываться с многочисленными заряженными группами белка. В таких условиях наблюдаемое в изоэлектрической точке равновесие зарядов частично обусловлено их компенсацией связавшимися с молекулой белка анионами и катионами.
Другие рефераты на тему «Биология и естествознание»:
Поиск рефератов
Последние рефераты раздела
- Влияние экологических факторов на разнообразие моллюсков разнотипных искусственных и естественных водоемов
- Влияние экологии водоемов на биологическое разнообразие фауны
- Влияние фтора и фторосодержащих соединений на здоровье населения
- Влияние факторов внешней среды на микроорганизмы
- Влияние физической нагрузки на уровень адренокортикотропного гормона, адреналина, кортизола, кортикостерона в сыворотке крови спортсменов
- Временные аспекты морфогенетических процессов. Эволюция путем гетерохронии
- Вопросы биоэтики
