Почвы как ионообменные сорбенты, особенности сорбции ионов свинца дерново-подзолистой супесчаной почвы
Железо в почвах одновременно входит в кристаллические решетки алюмосиликатов, в гётит FeOOH, гематит Fe2O3, в различные гидроксилы. По мере расхода наиболее растворимых соединений Fe3+ его концентрация поддерживается в почвенном растворе другими соединениями железа. Соединения кремния в почвенном растворе представлены ортокремневой кислотой H4SiO4 или ее полимерными формами, а в твердых фазах о
дновременно сосуществуют аморфный и кристаллический диоксид кремния SiO2 (кварц), минералы группы алюмосиликатов. В крупных песчаных фракциях почв преобладают каркасные алюмосиликаты, во фракции менее 1 мкм — слоистые алюмосиликаты, из них наиболее распространены монтмориллонит, каолинит и гидрослюды [7].
Особенно многочисленны в почвах соединения углерода. Практически всегда в почвенном воздухе есть диоксид углерода СО2, в почвенном растворе — угольная кислота, в степных и сухостепных почвах — СаСО3 и Na2CO3; это только минеральные соединения. Набор соединений в органическом веществе до сих пор не подсчитан, но в их число входят как низкомолекулярные соединения, начиная от метана СН4, аминокислот, простейших кислот жирного ряда, моносахаридов, и до высокомолекулярных соединений, представленных целлюлозой, лигнином, полипептидами. Особое место занимают так называемые специфические для почв гуминовые вещества [8]. При характеристике почв наиболее информативны не отдельные индивидуальные соединения, а их группы, то есть совокупность соединений со сходными строениями и свойствами. Такими группами могут быть моносахариды, аминокислоты (в почвах обнаруживают до 17 — 22 различных аминокислот), гуминовые кислоты, фульвокислоты. Вещества, входящие в одну группу, примерно одинаково участвуют в почвенно-химических реакциях [9].
Группы органических соединений подразделяются на фракции по характеру связи с минеральными соединениями, могут быть, например, гуминовые кислоты свободные, связанные с Са2+, Fe3+, алюмосиликатами и т.п. Сложность состава почв, большой набор химических соединений обусловливают возможность одновременного протекания различных химических реакций и способность твердых фаз почв поддерживать сравнительно постоянным состав почвенного раствора, откуда растения непосредственно черпают химические элементы. Эту способность поддерживать постоянным состав почвенного раствора называют буферностью почв. В природной обстановке буферность почв выражается в том, что при потреблении какого-либо элемента из почвенного раствора происходит частичное растворение твердых фаз и концентрация раствора восстанавливается. Если в почвенный раствор извне попадают излишние количества каких-либо соединений, то твердые фазы почв связывают такие вещества, вновь поддерживая постоянство состава почвенного раствора. Это иллюстрируют возможные переходы ионов К+ и трансформация калийсодержащих веществ в почве. Итак, действует общее правило: буферность почв обусловлена большим набором одновременно протекающих химических реакций между почвенным раствором и твердыми частями почвы Химическое разнообразие делает почву устойчивой в изменяющихся условиях природной среды или при антропогенной деятельности [7].
3 Кислотность почв
Обменные катионы участвуют также в формировании потенциальной кислотности почв. Такая кислотность встречается в кислых дерново-подзолистых, серых лесных, красноземных почвах. Проявляется она только при воздействии на почву солевого раствора, так же как и при обычной реакции катионного обмена. Отличие состоит в том, что потенциальная кислотность обусловлена только катионами Н+ и А13+:
ПН+ + КС1 --- ПН+HCl или ПА13+ + ЗКС1--- ПК3+ + А1С13
ПК3+ + А1С13 --- ПК3+ + А1(ОН)3 + ЗНС1.
Где П – почвенно-поглощающий комплекс
И в том и в другом случае в растворе появляется некоторое количество НС1, что и создает кислую реакцию среды.
Устраняют потенциальную кислотность довольно простыми приемами. Обычно к почве добавляют карбонат кальция (известь), который нейтрализует различные формы кислотности:
ПН2 + СаСО3 — ПCa2++Н2СО3 --- ПCa2+ +СО2+Н2О
Природная кислотность почв может быть вызвана органическими кислотами, попадающими в почву с растительными остатками или корневымивыделениями, диоксидом углерода в почвенном воздухе и поступлением азотной и серной кислот с кислыми дождями. Анализ химических равновесий показал, что роль СО2 в этом процессе более значительна, чем это представлялось раньше. Растворение СО2 приводит к образованию угольной кислоты Н2СО3. Сама по себе это довольно слабая кислота, но в почвенном воздухе доля СО2 много выше, чем в атмосферном; в последнем доля СО2 составляет около 0,03%, а в почвенном воздухе достигает целых процентов. Поэтому в некарбонатных почвах только за счет СО2 величина рН может опускаться до 4,5 и даже ниже [4].
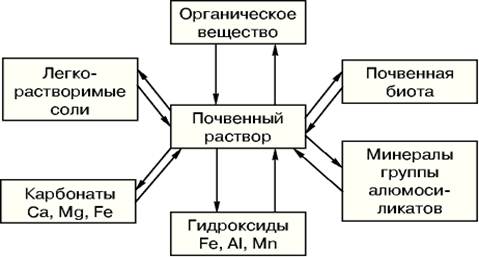
Рисунок 7- Реакция взаимодействия между почвенным раствором и другими компонентами почвы [4]
4 Окислительно-востановительный потенциал почвы
Практически в каждой почве происходят реакции окисления или восстановления химических соединений или элементов. Эти реакции являются сопряженными, и если какой-либо компонент почвы окисляется, то другой неизбежно восстанавливается. Окислительные процессы идут за счет кислорода воздуха, при этом органические вещества почвы окисляются или частично, или полностью до конечных продуктов распада — Н2О и СО2. При высоких окислительно-восстановительных потенциалах порядка 0,5 — 0,7 В практически все элементы с переменной валентностью приобретают высшие степени окисления, многие из них становятся малоподвижными и малодоступными растениям. Таковы ионы железа, меди, кобальта, серы, азота. Исключение составляет марганец, для перевода которого из Мп2+ в Мп7+ необходимы потенциалы около 1,4 — 1,5 В, тогда как даже в наиболее аэрированных и малоувлажненных почвах максимальные значения потенциалов редко превышают 0,6 — 0,7 В [19] .
В переувлажненных почвах, особенно в затопляемых рисовых почвах, развиваются восстановительные процессы, потенциалы снижаются до +0,2 -0,2 В, что обусловлено деятельностью микроорганизмов, способных развиваться без доступа свободного О2 и выделяющих в почву органические восстановленные соединения и свободный водород. В таких почвах элементы с переменной валентностью переходят в состояние низших степеней окисления, становятся подвижными, выделяется метан СН4, другие углеводороды. Когда длительно развиваются восстановительные процессы, в почвах появляется сизоватая окраска, железо и марганец восстанавливаются до Fe2+ и Мп2+. Такие почвы называют оглеенными или глеевыми. Кстати, переувлажненные или орошаемые и затопляемые почвы служат одним из важнейших природных источников выделения в атмосферу метана и других углеводородов, вызывающих проявления "парникового" эффекта [4].
5 Механизмы катионного обмена, особенности адсорбции
Содержание тяжелых металлов в почвенном растворе и доступность их для растений, в значительной мере, зависит от адсорбционных свойств почвы, Высокая адсорбционная активность почв способствует большему закреплению металлов и снижению их подвижности.
Другие рефераты на тему «Экология и охрана природы»:
Поиск рефератов
Последние рефераты раздела
- Влияние Чекмагушевского молочного завода на загрязнение вод реки Чебекей
- Влияние антропогенного фактора на загрязнение реки Ляля
- Киотский протокол - как механизм регулирования глобальных экологических проблем на международном уровне
- Лицензирование природопользования, деятельности в области охраны окружающей среды и обеспечения экологической безопасности
- Мировые тенденции развития ядерной технологии
- Негативные изменения состояния водного бассейна крупного города под влиянием деятельности человека
- Общественная экологическая экспертиза и экологический контроль
