Оптимизация ректификации фракции этан-пропен-пропан в простых и сложных колоннах
Пропан также представляет собой бесцветный газ, который растворим в органических растворителя и не растворим в воде. Его применяют как топливо для двигателей внутреннего сгорания, для получения сажи, в смеси с бутаном в баллонах используют как топливо в быту.
Пропен при обычных условиях является газом. Главным способами получения в промышленности пропена служат процессы расщепления нефтяных
фракций или углеводородных газов (каталитический и термический крекинги, пиролиз). Кроме того, пропен получают дегидрированием пропана. Ввиду своей реакционной способности пропен занял одно из ведущих мест как исходное вещество для органического синтеза.
Изначально, компоненты исследуемой смеси входят в состав широкой фракции легких углеводородов, получаемые в процессе нефтедобычи. Она содержит довольно широкий спектр углеводородов состава C1 - C7 которые в дальнейшем разделяются на узкие фракции:
• метан - водородную
• метан - этановую
• этан - этиленовую
• пропан - пропиленвую
• изопентановую
• гексановую и другие.
Для исследования применимости сложных колонн нами была выбрана простейшая из многокомпонентных смесей, не образующая азеотропов. Фракция этан-пропен-пропан оказалась в этом отношении весьма подходящей.
Модели парожидкостного взаимодействия
Модель NRTL
Уравнение NRTL (non-random two-liquid - неслучайное двужидкостное) было разработано Реноном и Праузницем с целью использовать концепцию локального состава, для избежания неспособности уравнения Вильсона к предсказанию разделения фаз жидкость — жидкость. Полученное в результате уравнение оказалось довольно хорошим для описания широкого диапазона систем, в высокой степени неидеальных смесей и для частично несмешивающихся систем. Выражение для коэффициента активности имеет вид:
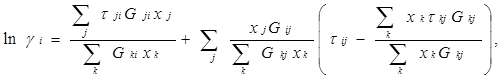 (8)
(8)
![]() где: (когда единицей измерения является °К):
где: (когда единицей измерения является °К):
Результирующее уравнение определяет коэффициент активности жидкости для каждой бинарной пары с точки зрения трех параметров. Выражения для параметров могут быть расширены с целью включения в них зависимости от температуры. В зависимости от выражений, использованных для параметров, уравнение может иметь три, пять, шесть или восемь параметров.
Модель Соав-Редлих-Квонг (SRK)
В 1972 г. для улучшения предсказания парового давления чистых компонентов и парожидкостного равновесия многокомпонентных смесей Соав предложил следующую температурную зависимость:
![]()
![]() (9)(10)
(9)(10)
где Tγ - приведенная температура, Т/Тс
ω — ацентрический фактор
Константы в уравнении (10) были получены из преобразования данных по паровому давлению для ограниченного числа обычных углеводородов. Эти пределы использования
уравнения состояния SRK ограничены неполярными компонентами.
Уравнение состояния Соав-Редлих-Квонга - это модификация уравнения состояния Редлиха-Квонга (которое основано на уравнении Ван-дер-Ваальса). Соав заменил член
a/T 0,5 более общей температурной зависимостью а(Т). Выражение получило следующий вид:
P = RT/(V-b)-a(T)/V(V + b)
![]()
![]() Где
Где ![]()
![]() , - критические температура и давление для i-ro компонента
, - критические температура и давление для i-ro компонента
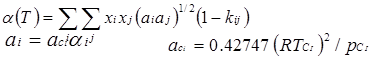 | |||||
![]() . — ацентрический фактор для компонента i
. — ацентрический фактор для компонента i
![]() - константа бинарного взаимодействия для компонентов i и j
- константа бинарного взаимодействия для компонентов i и j
Введение члена альфа позволило улучшить предсказание парового давления для чистых компонентов. Комбинированная формула для вычисления а(Т) с введенным членом ]$г означает улучшение предсказания свойств смеси.
Использование формулировки Соава для предсказания свойств смеси включает в себя два этапа. Во-первых, для каждого из компонентов подбирается ацентрический фактор компонента (ом) таким образом, чтобы точно предсказать давление паров компонента. Во-вторых, из экспериментальных данных для бинарных систем с компонентами i и j, для которых достигается фазовое равновесие, определяется параметр kij.
Модель Пенга-Робинсона
Уравнение состояния Пенга-Робинсона было опубликовано в 1976 году и является модификацией уравнения Редлиха-Квонга. Во многих отношениях оно похоже на уравненеие SRK, но все же он разработано для улучшения предсказания плотности жидкости. Как и в случае уравнения Соава-Редлиха-Квонга, в уравнении Пенга-Робинсона присутствует температурная зависимость а(Т) и выражение имеет следующий вид:
![]() где:
где:
- ![]()
![]() критические температура и давление для компонента i
критические температура и давление для компонента i
