Кондуктометрический метод анализа и его использование в анализе объектов окружающей природной среды
При соблюдении уравнения Я.И. Френкеля экспертные данные укладываются в прямолинейную зависимость ![]() . Отклонения свидетельствуют о структурных изменениях, которые могут быть связаны с разложением комплексных анионов на простые.
. Отклонения свидетельствуют о структурных изменениях, которые могут быть связаны с разложением комплексных анионов на простые.
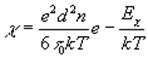 .
.
Контактные методы измерени
я электрической проводимости расплавов
В основе лежит закон Ома: на фиксированном участке проводника из жидкого металла, имеющего длину l и площадь поперечного сечения S, определяется электросопротивление Rχ.
Из соотношения ![]() устанавливают значения удельной электропроводимости металла.
устанавливают значения удельной электропроводимости металла.
Для определения электросопротивления проводника применяют следующие электрические измерительные схемы:
· схема вольтметра-амперметра, в которой при помощи вольтметра измеряют падение напряжения на концах проводника Vx, а амперметром – силу тока I. В этом случае значение Rx определяют по закону Ома: ![]() . Точность метода невысока (≤ 1%) и определяется классом точности приборов.
. Точность метода невысока (≤ 1%) и определяется классом точности приборов.
· Компенсационный метод: в цепь включают эталонное сопротивление Rэ и с помощью потенциометра измеряют падение напряжения на проводнике Vx и эталоне Vэ. Расчет по формуле: ![]() более точный метод.
более точный метод.
· С использованием моста Уитстона или двойного моста Томсона. Точность 0,2–0,3%, но необходимо учитывать контактные сопротивления и сопротивление проводов.
Определение электропроводимости расплавов связано с техническими трудностями: контакт расплава с электродами, подбор материалов.
Конструкции измерительных ячеек с различным расположением калиброванного канала, в котором проводник из жидкого металла, электроды токовые и потенциальные.
Для расчета удельного электрического сопротивления (или электрической проводимости) по измеренному (методом моста или методом вольтметра-амперметра) значению электрического сопротивления расплава необходимо знать константу ячейки. Градуировку ячейки обычно производят водным раствором (при комнатной температуре) или расплавом NaCl или KCl (при 700–900 °С).
Значение константы ячейки определяют по формуле:
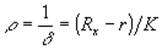 ,
,
где r – сопротивление проводящих проводов и электродов при соответствующих температурах опыта; Rx – измеряемое сопротивление.
Одним из способов определения r является предварительное определение.
Чаще используют другой метод, заключающийся в измерении электросопротивления при двух последовательных погружениях электродов на различную глубину. Этот способ позволяет исключить поправку на сопротивление проводов (r), т. к. расчет удельного электрического сопротивления ведут по разности измеренных сопротивлений:
![]() ,
,
где К1 и К2 – константы ячейки при двух последовательных погружениях электродов.
Конструкция установки разработанной Б.М. Лепинских и О.А. Есиным (УПИ) с мостовой схемой измерения и ячейкой типа электрод-электрод.
Регулирование глубины погружения электродов производится вращением стержня (#), при этом происходит подъем или опускание тигля при неподвижных электродах.
Среднее значение константы ячейки устанавливают градуированием по 0,1 н раствору KCl. Этот метод используется для определения электрической проводимости двойных шлаковых систем. Схема моста позволяет измерять сопротивление расплавов с точностью до 0,01 ом. Относительная ошибка определения удельной электрической проводимости двойных шлаковых систем. Схема моста позволяет измерять сопротивление расплавов с точностью до 0,01 ом. Относительная ошибка определения удельной электрической проводимости достигает 11,8%.
Кондуктометрия располагает несколькими законами:
1. В очень разбавленных растворах (предельно разбавленных) эквивалентная электропроводность (λ0) является постоянной характеристикой раствора, не зависящей от изменения концентрации электролита. Говоря простым языком, это означает, что в разбавленных растворах электропроводность прямопропорциональна количеству заряженных частиц – ионов.
Для растворов сильных электролитов область предельного разбавления простирается до концентрации 0,0001н, а с небольшой погрешностью можно считать границей предельного разбавления концентрацию 0,001н.
Для расчетов в области больших концентраций существует формула Кольрауша, но ее нельзя использовать для прогноза, поскольку она носит явно эмпирический характер:
λ = λ0 + K C 1/2,
2. Предельная эквивалентная электропроводность раствора электролита равна сумме эквивалентных электропроводностей катиона и аниона.
3. Эквивалентные электропроводности подавляющего числа ионов близки друг к другу по величине. Анализ экспериментальных данных показывает, что при 18 0С для катионов λ0=0,0053 ± 0,0019 Ом-1 м2 г-экв-1 и для анионов λ0=0,0055 ± 0,0027 Ом-1 м2 г-экв-1. При 25 0С λ 0=0,0062 ± 0,0023 Ом-1 м2 г-экв-1 для катионов и λ0=0,0064 ± 0,0031 для анионов. Исключение составляют ионы H+, OH-, Fe(CN)63-, Fe(CN)64-, электропроводности которых аномально высоки:
|
Ион |
Эквивалентная электропроводность, λ 0, Ом-1 м2 г-экв-1 | |
|
18 0С |
25 0С | |
|
H+ |
0,0315 |
0,03497 |
|
1/3 Fe(CN)63- |
- |
0,01009 |
|
1/4 Fe(CN)64- |
- |
0,01105 |
|
OH- |
0,0174 |
0,01976 |
4. Температура анализируемого раствора оказывает существенное влияние на измеряемые величины удельной электропроводности. В настоящее время не существует способа удовлетворительного описания влияния температуры на электропроводность. Причина такого положения дел кроется в слишком большом влиянии индивидуальной природы растворенных веществ на температурный коэффициент. С уверенностью можно сказать только одно: при повышении температуры на один градус удельная электропроводность раствора в среднем увеличивается на 1–2,5%.
Прямые кондуктометрические измерения
Аналитическое использование кондуктометрии обладает характерными чертами, связанными с низкой селективностью кондуктометрического детектирования. В самом деле, близкие значения эквивалентных электропроводностей ионов не позволяют говорить о том, что какой-либо ион может целиком определять электропроводность всего раствора. Таким образом, измерения электропроводности может приносить реальную аналитическую пользу только в том случае, если соотношение ионов в анализируемой смеси неизменно от пробы к пробе. Это, так называемая, задача определения разбавления исходного раствора. Примерами могут служить анализ промывных вод в ваннах отмывки гальванического производства, контроль за приготовлением технологических растворов в производственных условиях и т.п.
Другие рефераты на тему «Экология и охрана природы»:
Поиск рефератов
Последние рефераты раздела
- Влияние Чекмагушевского молочного завода на загрязнение вод реки Чебекей
- Влияние антропогенного фактора на загрязнение реки Ляля
- Киотский протокол - как механизм регулирования глобальных экологических проблем на международном уровне
- Лицензирование природопользования, деятельности в области охраны окружающей среды и обеспечения экологической безопасности
- Мировые тенденции развития ядерной технологии
- Негативные изменения состояния водного бассейна крупного города под влиянием деятельности человека
- Общественная экологическая экспертиза и экологический контроль
