Основные понятия молекулярной биологии
|
|
|
|
|
Рис.1 |
|
Рис.2 |
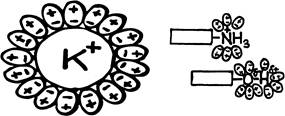
Если крупная молекула имеет на поверхности заряженную или поляризованную группу атомов, то вокруг нее тоже будут образовываться «местные» гидратные оболочки (рис. 2). Этого может быть достаточно для придания всей молекуле определенной (худшей, чем для чистого иона) растворимости в воде. К первому слою «прилипших» молекул воды такими же силами присоединяются еще слои молекул воды, образуется своего рода «шуба», которая «втягивает» молекулу в водное окружение, даже если остальные участки молекулы с водой не взаимодействуют.
Естественно, что сами диполи молекул воды электростатически и водородными связями притягиваются друг к другу. Это обусловливает, в частности, некоторую трудность испарения воды (по сравнению, например, с эфиром и спиртом). Вода «стремится» упорядочить расположение своих молекул по объему так, чтобы между ними образовалось максимальное число связей. Чем больше таких связей, тем меньше потенциальная энергия всей системы (ведь для разрыва связей, например испарения воды, надо подводить энергию нагревания). Любая подвижная система стремится занять положение, отвечающее минимуму потенциальной энергии. Тепловое движение молекул воды препятствует этому. Максимальное упорядочивание достигается лишь при 0°С, когда вода кристаллизуется в лед.
Гидрофобные молекулы образуются незаряженными и неполяризованными атомами и группами атомов. Они не связывают воду, не смачиваются. Таковы, например, алифатические цепочки вида СНз—CH2—CH2— . да и сами образующие их группы CH3— и —CH2— . Высока гидрофобность ароматических молекул: бензола (C6H6), фенола, толуола и других, в состав которых входят разного рода замкнутые циклы с сопряженными связями. Вода такие молекулы как бы «не замечает». Но, оказавшись в воде, несмачиваемые молекулы занимают место и мешают молекулам воды образовать максимально возможное при данной температуре число связей. Помехи уменьшатся, если гидрофобные молекулы соберутся в тесные кучки (капли), как показано на рис. 3, где кружками изображены гидрофобные молекулы, а зачерненными — молекулы воды.

Рис.3
Именно так вода «выталкивает» гидрофобные молекулы, точнее — сохраняет их случайное объединение. И хотя сами гидрофобные молекулы никак не взаимодействуют друг с другом, конечный результат выглядит так, будто они притягиваются некими силами, которые и условились называть «гидрофобными связями». Чтобы эти молекулы разъединить (растворить), надо затратить энергию на разрыв связей между молекулами воды, расчистить места для распределения гидрофобных молекул по всему объему. (Именно поэтому жир относительно легко смывается горячей водой).
Энергия разрыва таких связей, считая на моль гидрофобного вещества (при условии избытка воды) заметно больше, чем в случае ионной или водородной связи, а именно — около 2,4 ккал/моль. Но и она мала по сравнению с ковалентной связью. Так что гидрофобная связь тоже слабая.
Белковая глобула. Аминокислоты
Мы уже знаем, что все белки состоят из комбинации 20-ти аминокислот. Их можно получить из любой смеси белков гидролизом в 6М соляной кислоте при 110°Св течение суток без доступа воздуха (в запаянной ампуле). Методом хроматографии, — с которым мы в свое время познакомимся, — все 20 аминокислот, находящиеся в гидролизате можно разделить между собой. Упоминалось, что аминокислоты, образуя белок, выстраиваются в прочные цепи и что они обладают разного рода свободными, химическими группами атомов. Первое обстоятельство обеспечивается наличием во всех аминокислотах трехзвенной цепочки атомов, показанной на рис. 8. Прямоугольник и ромб там обозначают некие боковые ветви, строением которых аминокислоты отличаются друг от друга.
W-CH-COOH
Очевидно, в боковых ветвях и следует искать свободные группы атомов. Этим мы займемся немного позже. А сейчас посмотрим на доступные нашему вниманию трехчлены. На одном конце у них стоит аминогруппа (NHg), на другом — карбоксил (СООН), характерный для карбоновых кислот. Отсюда и название — аминокислоты.
Теперь приступим к рассмотрению боковых ветвей аминокислот. Для упрощения рисунка теперь уже цепочку трехчлена будем изображать в виде прямоугольника. Под ним — полное и сокращенное наименование аминокислоты, а во второй строчке — условное однобуквенное ее обозначение и молекулярный вес (дальтон). По химическим особенностям боковых ветвей аминокислоты можно разбить на несколько групп.
1. Аминокислоты, несущие электрический заряд (в воде):
а) основные: заряд положительный
б) кислые: заряд отрицателен
У аспарагина и глутамина в образовании водородных связей участвуют аминогруппы и атомы кислорода, а у серина и треони-на в этой роли выступают ОН-группы.
3. Аминокислоты, склонные к образованию гидрофобных связей:
а) алифатические;
б) ароматические
Заметное ультрафиолетовое поглощение растворов белков при 280 нм обусловлено главным образом поглощением трипто-фана, в меньшей степени — тирозина и совсем незначительно — фенилаланина.
4. Серусодержащие аминокислоты Эти аминокислоты не участвуют в образовании слабых связей. Для окончательной фиксации белковой глобулы неплохо было бы ее закрепить более прочными химическими «сшивками». Эту задачу берут на себя пары цистеинов. Сблизившись группами SH и вступив в реакцию окисления они образуют ковалентную связь между атомами серы Такую связь называют дисульфидным мостиком. Во многих белках дисульфидные мостики отсутствуют, в других их немного (3-6), но бывают и исключения. Например, в сывороточном альбумине быка их 17. Дисульфидную связь можно разорвать добавлением восстанавливающего агента, например, бета-мер-каптоэтанола (HS—С2Н5ОН).
Метионин, как мы увидим, играет особую роль в инициации синтеза белка.
5. Последняя аминокислота Пролин (Про) имеет особую структуру. Нарисуем ее формулу в полном виде . Собственно говоря, это не аминокислота, а иминокислота,так как вместо аминогруппы (NH3) в трехзвенной цепочке, стоит иминог-руппа (NH). Но это не мешает образовывать пептидную связь, имеющую вид, изображенный на рис. 17. Трехзвенная цепочка пролина не прямолинейна, а образует некий угол. Это обеспечивает изгиб цепи белка в том месте, где в ней находится пролин.
Все белки имеют одинаковый элементарный химический состав. Между тем, набор аминокислот у различных индивидуальных белков разный. Противоречие снимается, если вспомнить, что белковые цепи содержат сотни аминокислот. Суммарный состав усредняется до примерно следующих величин: 52% С; 22,5% О; 16% N; 7% Н; 1,5% S, по 1% Р и Fe (по весу). Фосфор и железо входят в состав не всех белков.
Другие рефераты на тему «Биология и естествознание»:
Поиск рефератов
Последние рефераты раздела
- Влияние экологических факторов на разнообразие моллюсков разнотипных искусственных и естественных водоемов
- Влияние экологии водоемов на биологическое разнообразие фауны
- Влияние фтора и фторосодержащих соединений на здоровье населения
- Влияние факторов внешней среды на микроорганизмы
- Влияние физической нагрузки на уровень адренокортикотропного гормона, адреналина, кортизола, кортикостерона в сыворотке крови спортсменов
- Временные аспекты морфогенетических процессов. Эволюция путем гетерохронии
- Вопросы биоэтики