Химический язык
Что такое электролиты? Почему электролиты являются участниками электролиза?
электролиз расплавоврастворов Правила определения продуктов электролиза расплавов и растворов электролитов (схемы представлены на каждого ученика).
I. Катодные процессы
электрохимический ряд напряжений металлов Li Rb K Ba Ca Na Mg Mn Zn Cr Fe Pb Cu Hg Ag Pt Au
восстановление H2Oвосстановление H2O и восст
ановление H2O + 2ê →H2 +2OH - металла Men+ + nê→Me0 металла усиление окислительных свойств катионов II. Анодные процессы
анионы
бескислородсодержащиекислородсодержащие галогенид-ионы OH - , NO3-, SO42-
2 Cl - - 2ê → Cl2↑ 2H2O - 4ê→O2+4H+; 4OH - - 4ê→O2+2H2O.
I - Br S2 - Cl - OH - SO42 - NO3 - F -
ослабление восстановительной способности анионов Применение электролиза: покрытие металлов; защита от коррозии; получение металлов и других соединений; очистка веществ от примесей.
Опираясь на правила, составим уравнение электролиза раствора иодида калия и расплава хлорида меди (II).
а) KI + H2O →
К (-): К+; H2O H2O + 2ê →H2 +2OH - восстановление А (+): I-; H2O2 I - - 2ê → I2 окисление 2KI + H2O → 2KOH + I2 + H2 ↑.
б) CuCl2 расплав→
К (-): Cu2+ Cu2+ + 2ê → Cu0 восстановление А (+): Cl- 2 Cl - - 2ê → Cl2↑ окисление CuCl2 расплав→ Cu0 + Cl2↑.
Вода не является участником процесса расплава веществ.
Итоги урока.
Домашнее задание: § 18, оформить записи, выполнить задание:
Составьте уравнение электролиза: а) раствора бромида железа (II); б) расплава оксида алюминия; в) раствора нитрата ртути; г) раствора иодида никеля (II); д) раствора серной кислоты. Подготовка к контрольной работе.
Фрагмент урока № 4
Тема: " Решение задач и упражнений по теме "Металлы".
Цель: Закрепит знания по теме, отработать умение составления уравнений реакций с участием металлов.
Ход урока:
Организация класса.
Проверка домашнего задания (12-15 мин).
Выполнение самостоятельной работы.
I вариант 1. Допишите уравнение реакции, расставьте коэффициенты методом электронного баланса и определите тип ОВР: а) Co+ HNO3(конц) → .
2. На рисунке изображен разрез хромированного железного листа. Определите, что такое 1 и 2, напишите схемы катодного и анодного процессов.
 |
3. Разделите вещества HNO3, KClO4, H2O2, Mg, NH3 на три группы:
1 - проявляющие только окислительные свойства;
2 - проявляющие только восстановительные свойства;
3 - проявляющие как окислительные, так и восстановительные свойства.
4. При электролизе раствора КОН на катоде выделится:
а) водород; б) кислород; в) калий?
5. При электролизе раствора хлорида бария на аноде выделяется:
а) водород; б) хлор; в) кислород?
Остальные варианты – приложение 2.
Приложение
Занимательные задания (оформление стендов в кабинете)
1. Поджигает … вода!
Если смешать порошок металла (цинка или алюминия) с измельченными кристаллами некоторого неметалла, а потом добавить каплю воды, начинается бурная окислительно-восстановительная реакция с выделением теплоты, света и фиолетовых паров. Что это за реакция?
2. Первые спички Немецкий химик Ян Каммерер работал учителем химии. В 1820 г. он
показал своим ученикам рискованный опыт. Смешав под водой воскообразное белое вещество с бесцветным кристаллами соли, полученной французским химиком Бертолле и названной его именем, он добавил клей, а потом погрузил в образовавшееся "тесто" пучок осиновых палочек. Затем палочки были извлечены из смеси и осторожно высушены. Каммерер раздал палочки своим подопечным и попросил провести ими по поверхности стола. Все палочки воспламенились, ученики были в восторге: ведь они держали в руках первые спички. Какие вещества использовал Каммерер?
3. Химический хамелеон
В ХIХ в. для химического анализа различных веществ применялся раствор "хамелеона". В исходном состоянии он был фиолетовым, а при реакциях с восстановителями в кислотной среде обесцвечивался. Если реакции протекали при большом избытке щелочи, раствор становился зеленым. А в нейтральной среде восстановители делали "хамелеона" буро-коричневым. О каком веществе идет речь?
4. Медные фокусы
В 1928 г. чешский химик И. Друце обнаружил, что, если медные стружки залить концентрированной серной кислотой и нагреть до 2000C, получается раствор зеленого цвета. При смешивании этого раствора с безводным метанолом (метиловым спиртом) выпадает белый осадок. Друце попытался растворить этот осадок в воде и получил раствор голубого цвета, а на дне сосуда оказались крупинки металлической меди. Какое вещество получил Друце?
5. Алюминий подвел!
Железную водосточную трубу закрепили на стене дома хомутами из алюминиевого сплава. Через несколько лет во время сильного дождя труба рухнула на тротуар. Оказалось, что крепежные детали из алюминиевого сплава подверглись сильной коррозии, хотя кровля дома, сделанная из того же сплава, безупречно служила уже полтора десятка лет, Почему так сильно отличалось поведение алюминиевых изделий?
6. Обновили! .
Серебряные столовые приборы часто украшают "черненым" рисунком. Подобные узоры можно встретить и на мельхиоровых ложках, вилках и ножах. Однажды после званого ужина все ложки, вилки и ножи, залив мыльной водой, оставили в тазике из оцинкованного железа. Наутро оказалось, что все приборы из серебра и мельхиора стали белыми как снег, а столь ценный "черненый" рисунок пропал. Что же произошло?
7. Химическая "угадай-ка"
В руки учеников попали обрывки бумаги - черновики учителя, готовившего задания для контрольной работы. Все коэффициенты в уравнениях реакций были поставлены правильно. какие же вещества вступили в реакции, если получились следующие продуты:
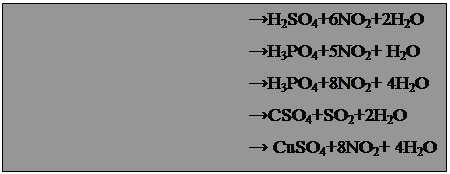
8. Ошибка лаборанта Для получения сероводорода на лекциях использовали аппарат Киппа с кусочками сульфида железа и разбавленной соляной кислотой. Но вот на очередную лекцию лаборант вынес аппарат, все внутренние стенки которого были покрыты беловато-желтым налетом, а вместо прозрачного раствора кислоты пузырилась мутная, слегка желтоватая жидкость. Профессор потребовал немедленно унести аппарат и перезарядить его, так как вместо разбавленной соляной в нем оказалась серная кислота, к тому же концентрированная. Что произошло в аппарате Киппа?
Другие рефераты на тему «Химия»:
- Полярные диаграммы и энергетические уровни волновых функций жесткого ротатора
- Физико-химические основы активации электродов, работающих по принципу электрохимического внедрения для литиевого аккумулятора
- Энтропия полимерной цепи
- Белки и нуклеиновые кислоты
- Частицы и коллектив. Неразличимость и симметрия Коррекция статистических сумм для трансляции и ротации
