Производство азотной кислоты
Механизм гетерогенного каталитического окисления аммиака состоит из следующих последовательных стадий:
—диффузия молекул аммиака и кислорода из газовой фазы к поверхности катализатора;
—активированная адсорбция молекул кислорода на поверхности катализатора с образованием промежуточного соединения;
—хемосорбция молекул аммиака и образование комплекса;
—разложение комплекса с реге
нерацией катализатора и образованием молекул оксида азота (II) и воды;
—диффузия продуктов реакции с поверхности катализатора в газовую фазу.
Определяющей стадией всего процесса окисления является скорость диффузии кислорода к поверхности катализатора. Следовательно, каталитическое окисление аммиака на платиновом катализаторе протекает преимущественно в диффузионной области, в отличие от окисления на окисном катализаторе, которое идет в кинетической области.
Платиновые катализаторы весьма чувствительны к каталитическим ядам, содержащимся в аммиаке и воздухе, образующим аммиачно-воздушную смесь (АмВС). Фосфористый водород вызывает его необратимое, а ацетилен, сероводород и органические соединения серы обратимое отравление. Так как вследствие этого активность катализатора снижается, его периодически регенерируют промывкой соляной или азотной кислотой.
В процессе работы поверхность катализатора разрушается и частицы его уносятся с потоком газа. Эррозия катализатора тем больше, чем выше температура, давление и объемная скорость газа, проходящего через катализатор. Для систем, работающих под высоким давлением, унос катализатора составляет 0,3—0,4 г на 1 тонну азотной кислоты.
В присутствии платиновых катализаторов селективность процесса окисления аммиака до оксида азота (II):
![]() (5)
(5)
составляет 0,95—0,98 дол, ед. В этих условиях скорость окисления до оксида азота (II) описывается уравнением:
![]() (6)
(6)
где: ![]() — парциальное давление аммиака, окисляемого до оксида азота (II),
— парциальное давление аммиака, окисляемого до оксида азота (II),
![]() — парциальное давление аммиака, окисляемого до оксида азота (I) и элементарного азота (реакции2иЗ),
— парциальное давление аммиака, окисляемого до оксида азота (I) и элементарного азота (реакции2иЗ),
к — константа скорости.
Энергия активации этой реакции составляет 33,494 кДж/ моль.
Из двух реакций (2 и 3), конкурирующих с целевой реакцией окисления аммиака (1), наиболее опасной является реакция 3, приводящая к образованию элементарного азота. Скорость обеих реакций (1 и 3) может быть описана общим для гетерогенных реакций уравнением:
![]() (7)
(7)
и зависит от таких параметров процесса как температура (через Км), давление и состав АмВС, то есть отношение кислород: аммиак (через АС), время контактирования, то есть время пребывания АмВС в зоне катализатора. Влияние этих факторов на скорость окисления аммиака до оксида азота (II) по реакции 1 и до азота по реакции 3 и, следовательно, выход продуктов окисления, различно.
4.1. Температура. Повышение температуры способствует увеличению скорости реакций и коэффициента диффузии аммиака в смеси и, поэтому, является наиболее эффективным средством, увеличения скорости процесса, протекающего преимущественно в диффузионной области. Это подтверждается термодинамическими данными табл. 15.1.
Термодинамические характеристики реакций окисления аммиака
Таблица 4.1.
| Реакция | ΔН, Дж/моль | AG, кДж/моль | |
| 298°К | 1173оК | ||
|
4NH3 + 502 = 4NO + 6Н20 | -226,0 | -246,2 | -414,6 |
|
4NH3 + 302 = 2Н2 + 6Н20 | -317,2 | -326,9 | -335,2 |
Из таблицы следует, что вероятность реакции окисления до оксида азота (II) с повышением температуры возрастает почти вдвое, а реакции окисления до азота почти не изменяется. Зависимость выхода оксида азота (II) и элементарного азота от температуры представлена на рис. 4.1.
4.2. Состав АмВС, Соотношение аммиака и кислорода в газовой смеси влияет на температурный режим и общую скорость процесса в том случае, если лимитирующей в нем является химическая реакция, то есть процесс протекает в кинетической области. При стехиометрическом соотношении компонентов в АмВС степень превращения аммиака в оксид азота (II) не превышает 0,65 дол. ед. Для увеличения выхода оксида азота (II) процесс ведут при отношении О2 : NH3 = 1,8—2,0, что соответствует содержанию в АмВС 0,095—0,105 об. долей аммиака и 0,18—0,19 об. долей кислорода. Избыток кислорода используется на стадии доокисления оксида азота (II), а указанный состав АмВС обеспечивает автотермичность процесса окисления и лежит за пределом взрывчатости АмВС. Зависимость выхода оксида азота (II) от состава АмВС представлена на рис. 4.2.
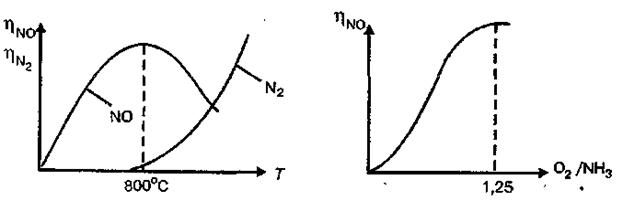
Рис. 4.1. Зависимость выхода NO и N2 Рис. 4.2. Зависимость выхода NO от температуры от состава АмВС
3. Давление. Повышение давления ускоряет процесс окисления аммиака за счет увеличения концентрации реагентов и производительности катализатора, что позволяет сократить размеры аппаратуры. При этом, однако, снижается выход оксида азота (II) и увеличивается эрозия и унос катализатора, что удорожает продукцию. Так, если при атмосферном давлении (105 Па) унос катализатора не превышает 0,05 г на тонну азотной кислоты, то при давлении 0,8 МПа он достигает 0,4 г/тонну. Зависимость выхода оксида азота (II) от давления при различной температуре приведена на рис. 4.3.
4. Время контактирования, Скорость каталитического окисления аммиака до оксида азота (II) весьма высока. За десятитысячные доли секунды степень превращения составляет 0,9 7— 0,98 дол. ед. при атмосферном давлении и 0,98—0,96 при давлении 0,8—1,0 МПа. Время контактирования может быть рассчитано из формулы:
![]() (8)
(8)
где: Vk — объем катализатора, определяемый в случае платинового катализатора числом сеток в пакете, W — объемная скорость АмВС. Время контактирования зависит от природы катализатора и составляет; для платиновых катализаторов 10-4 - 10-5с, для окисных катализаторов около
10-2с. Увеличение времени контактирования, то есть снижение объемной скорости АмВС приводит к развитию реакции окисления аммиака до элементарного азота (рис. 4.4.).