Коррозия и защита металлов
При рассмотрении кинетики коррозионных процессов в растворе электролитов до сих пор принималось, что процесс в основном протекает по электрохимическому механизму, так как скорость коррозии по химическому механизму (т.е. прямому взаимодействию окислителя с металлом) мала. Однако было установлено, что некоторые металлы (железо, хром) в растворах некоторых кислот (например, НСl) могут корродироват
ь с высокими скоростями по химическому механизму.
Таким образом, электрохимическая коррозия протекает через сопряженные процессы анодного растворения металла и катодного восстановления окислителя, обычно молекул кислорода или ионов водорода. Возможность протекания при коррозии того или иного катодного процесса определяется его потенциалом. Коррозия с поглощением кислорода лимитируется стадией диффузии кислорода и возрастает с увеличением его концентрации и при перемешивании и зависит от температуры. Коррозия с выделением водорода зависит от природы примесей в металле, от рН и возрастает с увеличением температуры. Некоторые металлы имеют склонность к пассивации вследствие образования защитных слоев.
Защита металлов от коррозии
В соответствии с рассмотренными ранее механизмами коррозию металлов можно затормозить изменением потенциала металла, пассивацией металла, снижением концентрации окислителя, изоляцией поверхности металла от окислителя, изменением состава металла и др. При разработке методов защиты от коррозии используют указанные способы снижения скорости коррозии, которые меняются в зависимости от характера коррозии и условий ее протекания. Выбор способа определяется его эффективностью, а также экономической целесообразностью. Все методы защиты условно делятся на следующие группы: а) легирование металлов; б) защитные покрытия (металлические, неметаллические); в) электрохимическая защита; г) изменение свойств коррозионной среды; д) рациональное конструирование изделий.
Легирование металлов. Это эффективный (хотя и дорогой) метод повышения коррозионной стойкости металлов. При легировании в состав сплава вводят компоненты, вызывающие пассивность металла. В качестве таких компонентов применяют хром, никель, вольфрам и др.
Широкое применение нашло легирование для защиты от газовой коррозии. Введение некоторых добавок к сталям (титана, меди, хром и никеля) приводит к тому, что при коррозии образуются плотные продукты реакции, предохраняющие сплав от дальнейшей коррозия. При этом используют сплавы, обладающие жаростойкостью и жаропрочностью.
Жаростойкость - стойкость по отношению к газовой коррозии при высоких температурах. Жаропрочность - свойство конструкционного материала сохранять высокую механическую прочность при значительном повышении температуры. Жаростойкость обычно обеспечивается легированием металлов и сплавов, на пример, стали хромом, алюминием и кремнием. Эти элементы при высоких температурах окисляются энергичнее, чем железо, и образуют при этом плотные защитные пленки оксидов, например, ![]() ,
, ![]() и
и ![]() . Хром и кремний улучшают также жаропрочность сталей. Стали, легированные 4-9% хрома, молибденом или кремнием применяют, например, в парогенераторо- и турбостроении. Сплав содержащий 9 - 12% хрома, применяют для изготовления лопаток газовых турбин, деталей реактивных двигателей, в производстве двигателей внутреннего сгорания и т.п.
. Хром и кремний улучшают также жаропрочность сталей. Стали, легированные 4-9% хрома, молибденом или кремнием применяют, например, в парогенераторо- и турбостроении. Сплав содержащий 9 - 12% хрома, применяют для изготовления лопаток газовых турбин, деталей реактивных двигателей, в производстве двигателей внутреннего сгорания и т.п.
Сплавы Сr-А1-Fе обладают исключительно высокой жаростойкостью. Например, сплав, содержащий 30% Сr, 5% А1, 0,5% Si, устойчив на воздухе до 1300°С. Эти сплавы используют, в частности, в качестве материала дня изготовления спиралей и деталей нагревательных элементов печей сопротивления. К их недостаткам относятся низкая жаропрочность и склонность к хрупкости при комнатной температуре после продолжительного нагрева на воздухе, вызываемая в известной степени образованием нитридов алюминия. По этой причине положение спиралей в печах должно быть фиксировано, а для беспрепятственного термического расширения и сжатия спирали обычно гофрируют. Жаростойкость никеля еще больше повышается при добавлении хрома. Сплав, содержащий 20% Сr и 80% Ni, устойчив на воздухе до 1150 ![]() C. Этот сплав - один из лучших жаростойких и жаропрочных сплавов.
C. Этот сплав - один из лучших жаростойких и жаропрочных сплавов.
Легирование также используется с целью снижения скорости электрохимической коррозии, особенно коррозии с выделением водорода. К коррозионно-стойким сплавам, например, относятся нержавеющие стали, в которых легирующими компонентами служат хром, никель и другие металлы.
Защитные покрытия. Слои, искусственно создаваемые на поверхности металлических изделий и сооружений для предохранения их от коррозии, называются защитными покрытиями. Если наряду с защитой от коррозии покрытие служит также для декоративных целей, его называют защитно-декоративным. Выбор вида покрытия зависит от условий, в которых используется металл.
Металлические покрытия. Материалами для металлических защитных покрытий могут быть как чистые металлы (цинк, кадмий, алюминий, никель, медь, хром, серебро и др.), так и их сплавы (бронза, латунь и др.). По характеру поведения металлических покрытий при коррозии их можно разделить на катодные и анодные. К катодным покрытиям относятся покрытия, потенциалы которых в данной среде имеют более положительное значение, чем потенциал основного металла. В качестве примеров катодных покрытий на стали можно привести Сu, Ni, Аl. При повреждении покрытия (или наличии пор) возникает коррозионный элемент, в котором основной материал в поре служит анодом и растворяется, а материал покрытия - катодом, на котором выделяется водород или поглощается кислород (рис.8, а). Следовательно, катодные покрытия могут защищать металл от коррозии лишь при отсутствии пор и повреждений покрытия. Анодные покрытия имеют более отрицательный потенциал, чем потенциал основного металла. Примером анодного покрытия может служить цинк на стали. В этом случае основной металл будет катодом коррозионного элемента, поэтому он не корродирует (рис.8, б). Потенциалы металлов зависят от состава растворов, поэтому при изменении состава раствора может меняться и характер покрытия. Так, покрытие стали оловом в растворе ![]() - катодное, а в растворе органических кислот - анодное.
- катодное, а в растворе органических кислот - анодное.
Для получения металлических защитных покрытий применяются различные способы: электрохимический (гальванические покрытия), погружение в расплавленный металл, металлизация, термодиффузионный и химический. Из расплава получают покрытие цинка (горячее цинкование) и олова (горячее лужение).
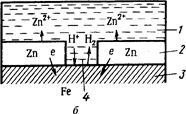
Рис.8. Схема коррозии железа в кислотном растворе в порах катодного (а) анодного (б) покрытий: 1 - раствор; 2 - покрытие; 3 - основной металл; 4 – пора.
Металлизация - способ получения металлических защитных покрытий на различных сооружениях (мосты, детали судов, большие баки и др.); при этом способе расплавленный металл с помощью струи сжатого воздуха наносится на защищаемую поверхность. Этим методом можно получать слои почти любой толщины и с хорошим сцеплением с основным металлом. К преимуществам этого способа относится возможность нанесения покрытия на собранные конструкции. Иногда для повышения коррозионной стойкости пор покрытия заполняют термопластичными смолами.
