Транспорт субстратов и продуктов

Системы второго типа, в свою очередь, подразделяются на системы "первичного" активного транспорта, генерирующие ТЭП и системы "вторичного" активного транспорта, использующие ТЭП для транспорта органических и неорганических субстратов. В некоторых случаях, например в системах со "связывающим
и" белками, энергия АТР непосредственно используется в транспорте субстратов. Системы "вторичного" активного транспорта распространены более широко и могут функционировать в соответствии с тремя основными механизмами.
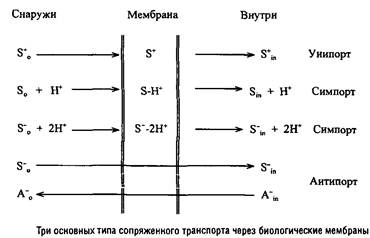
Катионы транслоцируются в клетку по градиенту электрического потенциала путем своеобразного электрофореза.
Незаряженные соединения транслоцируются в клетку совместно с катионами Н+ или Na+.
Анионы также могут транслоцироваться в клетку путем сим-порта, присоединяя такое количество катионов, которого достаточно для перевода комплекса субстрата с переносчиком в положительно заряженную форму. Кроме того, анионы внешней среды могут обмениваться на внутриклеточные анионы. По механизму антипорта могут транслоцироваться и катионы, например у прокариот широко распространена система антипорта Н+ и Na+, а у эукариот - система антипорта К+ и Na+.
Регуляция транспортных процессов
Как и регуляция процессов внутриклеточного метаболизма, она осуществляется на двух уровнях: на уровне биосинтеза белковых посредников и на уровне функционирования готовых посредников.
Основными механизмами регуляции биосинтеза переносчиков транспортных систем являются индукция, репрессия и катаболитная репрессия.
Как и в случае ферментов, по типу индукции и катаболитной репрессии регулируется биосинтез компонентов тех транспортных систем, субстраты которых участвуют в процессах катаболизма. По типу репрессии избытком субстрата регулируется главным образом биосинтез аминокислотных транспортных систем.
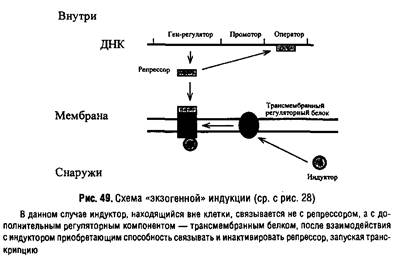
Особенность регуляции некоторых транспортных процессов состоит в том, что индукция осуществляется не внутриклеточным субстратом, а внеклеточным субстратом.
Такая индукция называется экзогенной и требует наличия промежуточного регуляторного интегрального мембранного белка, передающего сигнал индуктора на репрессор.
Подобный тип индукции характерен, например, для транспортной системы гексозофосфатов, фосфоглицерата, некоторых трикарбоновых кислот, а также компонентов фосфотрансферазной системы.
Картина регуляции осложняется тем, что у многих организмов для одного и того же субстрата часто используется несколько транспортных систем, отличающихся по специфичности и величине кинетических параметров. Существуют системы с узкой специфичностью, предназначенные только для одного или небольшого числа сходных субстратов, и с широкой специфичностью. Например, у Escherichia coli существуют четыре системы для транспорта ароматических аминокислот: три из них специфичны только для одной из этих аминокислот, а четвертая является общей для всех.
Регуляция активности белковых посредников транспортных систем может осуществляться способом обратимой ковалентной модификации или путем нековалентного взаимодействия с эффекторами. В последнем случае, если эффектор взаимодействует с транспортной системой, находясь на той же стороне мембраны, что и субстрат, говорят о цис-регуляции. Например, отрицательная цис-кооперативность обнаруживается при транспорте пролина у Escherichia coli: избыток субстрата тормозит свой собственный транспорт из среды. У галобактерий, наряду с обычными четырьмя транспортными системами для ароматических аминокислот, существует высокоспецифичная - для тирозина, обладающая очень высоким сродством к субстрату, активность которой подавляется избытком тирозина по бесконкурентному типу.
Если эффектор взаимодействует с транспортной системой, находясь по разные стороны мембраны относительно субстрата, говорят о транс-регуляции транспорта. Например, некоторые аминокислоты, в частности ароматические, находясь внутри клетки, тормозят свой собственный транспорт из среды.
События, связанные с регуляцией транспортных процессов, иногда оказывают существенное влияние на процессы метаболизма в целом. Ярким примером является участие фосфотрансферазной системы в регуляции биосинтеза белков по типу катаболитной репрессии. Оказалось, что уровень сАМР у Escherichia coli облигатно зависит от функционирования фосфотрансферазной системы, причем главную роль в этой связи играет специфический для глюкозы компонент Е 111.
В отсутствие глюкозы все компоненты системы, в том числе и Е I 11, находятся в фосфорилированном состоянии за счет резерва PEP. Фосфорилированный Е 111, взаимодействуя с аденилатциклазой, переводит ее в активное состояние, в результате чего внутриклеточный уровень сАМР повышается и активируется транскрипция "слабых" оперонов, в том числе систем транспорта и метаболизма других Сахаров.
Напротив, в присутствии глюкозы степень фосфорилирования Е I 11 снижается в связи с переносом фосфорильного остатка на глюкозу в процессе ее транспорта. В результате уменьшается активность аденилатциклазы, снижается уровень сАМР и блокируется транскрипция ряда "сахарных" оперонов.
Следует добавить, что нефосфорилированная форма Е I I I, по-видимому, может инактивировать транспортные системы других Сахаров, предотвращая поступление последних в клетку, что еще более усиливает катаболитную репрессию.
Каков же механизм катаболитной реперессии в случае, когда подавляется синтез ферментов, ответственных за катаболизм самой глюкозы, а в качестве более выгодных в энергетическом смысле субстратов выступают, например, органические кислоты или водород?
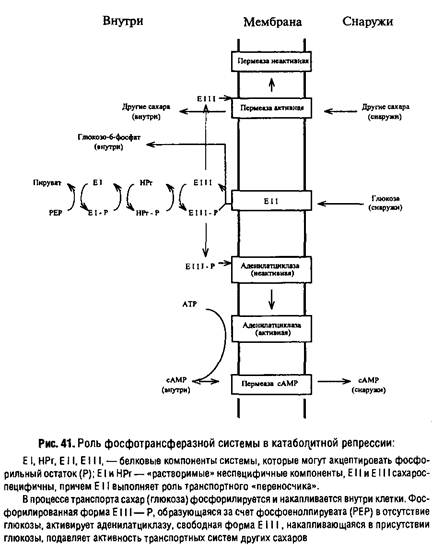
Ведь тогда участие фосфотрансферазной системы невозможно. Чтобы понять механизм явления, необходимо обратить внимание на нижнюю часть рис.41, где изображена система экскреции сАМР. Значение этих систем для регуляции метаболизма мы рассмотрим подробнее в следующем параграфе, а здесь отметим только, что одним из способов снижения уровня сАМР может служить активирование его выброса из клетки, например наложением на мембрану ТЭП, т.е. путем "энергизации" мембраны, степень которой, естественно, будет выше всегда, когда используется более выгодный в энергетическом отношении субстрат. Таким образом, если субстрат обеспечивает энергетические потребности клетки и создает необходимую степень "энергизации" мембраны, он может вызывать подавление использования других субстратов, от которых зависит уровень с AMP в клетке.
Транспорт веществ из клетки в среду: секреция и экскреция
Рассмотрим сначала процессы секреции, т.е. выделение из клетки белков.
Секретируемые белки синтезируются в виде более длинных предшественников, которые подвергаются процессингу, как правило, на этапе транслокации через мембрану. Они содержат на NHj-конце так называемый сигнальный пептид из 15-30 аминокислот, которые удаляются специальной сигнальной пептидазой, локализованной в мембране. Транслокация белка через мембрану обычно протекает одновременно с трансляцией, хотя известны случаи посттрансляционной транслокации. После образования сигнального пептида трансляция временно прекращается в результате присоединения к рибосоме нуклеопротеидного ингибитора и полисомный комплекс перемещается к мембране, где локализован аппарат секреции, включающий рецепторы рибосомы и сигнального пептида. Происходит формирование трансмембранной "поры". Сигнальный пептид закрепляется на своем рецепторе, и трансляция возобновляется, причем растущая пептидная цепь "проталкивается" через мембрану. Сигнальный пептид отщепляется сигнальной пептидазой, и "зрелая" молекула фермента отделяется от рибосомы. После завершения трансляции рибосомный комплекс покидает мембрану и диссоциирует на субчастицы для подготовки нового цикла трансляции.
Другие рефераты на тему «Биология и естествознание»:
Поиск рефератов
Последние рефераты раздела
- Влияние экологических факторов на разнообразие моллюсков разнотипных искусственных и естественных водоемов
- Влияние экологии водоемов на биологическое разнообразие фауны
- Влияние фтора и фторосодержащих соединений на здоровье населения
- Влияние факторов внешней среды на микроорганизмы
- Влияние физической нагрузки на уровень адренокортикотропного гормона, адреналина, кортизола, кортикостерона в сыворотке крови спортсменов
- Временные аспекты морфогенетических процессов. Эволюция путем гетерохронии
- Вопросы биоэтики
