Исследование твердых электролитов
Внешне мембрана "Nafion" представляет собой оптически прозрачные в видимой части спектра листы толщиной от 0,1 до 1 мм. Вследствие инертности своей фторуглеродной основы этот ТПЭ чрезвычайно устойчив к химическим воздействиям (выдерживает кипячение в концентрированной азотной кислоте), механически прочен и термически устойчив (до 100°С). Обычно он выпускается в протонированной или нат
риевой форме (K = H + или Na + соответственно). Эквивалентная масса "Nafion" составляет от 900 до 1200 г в расчёте на эквивалент сульфогрупп.
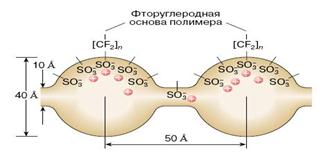
Рис. 1. Внутренняя структура ТПЭ "Nafion"
Исследования внутреннего строения ТПЭ "Nafion" показали, что он имеет двухфазную структуру (рис. 1). Основа полимера (гидрофобная фаза) состоит из фторуглеродных и эфирных цепей, расположенных в пространстве таким образом, что функциональные сульфогруппы группируются внутри сферических полостей диаметром порядка 40 Å. Система связанных узкими каналами полостей, содержащих гидратированные катионы, представляет собой вторую, гидрофильную фазу мембраны.
Перенос заряда в ТПЭ осуществляется в простейшем случае за счёт перехода катионов с одной сульфогруппы на другую. Специальными исследованиями было установлено, что небольшие по размеру катионы могут легко переходить из одной полости в другую, тогда как движение анионов через узкие каналы затруднено из-за отталкивания от одноимённо заряженных функциональных групп. Это свойство определяет возможность использования "Nafion" как ион-селективных мембран, способных пропускать одни ионы и задерживать другие.
Главной особенностью "Nafion" является её чрезвычайно высокая ионная проводимость. Величину проводимости ТПЭ или, другими словами, скорость транспорта заряда через них принято оценивать через коэффициент диффузии заряженных частиц (коэффициент диффузии заряда) D (см 2/c). Коэффициент диффузии ионов Na + в мембране "Nafion" составляет около 1·10 –6 см 2/c, что сравнимо с коэффициентом диффузии этих ионов в концентрированном водном растворе хлорида натрия.
Рассматриваемые полимеры, подобно ионообменным смолам, способны обменивать входящие в их состав катионы на катионы внешней среды. Методом ионного обмена в ТПЭ можно внедрять как простые, так и достаточно крупные комплексные катионы типа [Ru(bipy)3] 2+ , где bipy = 2,2'-бипиридин. При этом концентрация катионов в мембране может превышать предельно возможную концентрацию данных катионов в растворе. Так, после выдерживания мембраны в водном растворе, содержащем 10 –3 моля [Ru(bipy)3] 2+ на литр, концентрация этих ионов в ТПЭ может быть в 500–700 раз больше. Причём внедрённые комплексные катионы прочно удерживаются мембраной: уменьшения концентрации комплекса не было обнаружено даже после промывки мембраны в проточной воде в течение нескольких дней.
Полимеры с эквивалентной массой 900–1000 г/экв могут медленно растворяться в этаноле или диметилформамиде. Это свойство является весьма важным, поскольку даёт возможность получать на поверхности электродов различных электрохимических систем тонкие плёнки ТПЭ путём нанесения раствора и выпаривания растворителя при небольшом нагревании. Такие электроды с тонким слоем ТПЭ на поверхности и введённым в полимер для придания электроду каких-либо специфических свойств ЭАВ называют полимерными электродами. Они, в свою очередь, относятся к классу химически модифицированных электродов (ХМЭ). Химически модифицированными называют электроды, на поверхность которых нанесены молекулярно организованные химические системы, предназначенные для целенаправленного изменения электрохимических, каталитических или оптических свойств электрода.
Краткое рассмотрение свойств ТПЭ "Nafion" позволяет выделить основные направления его практического использования (рис. 2).
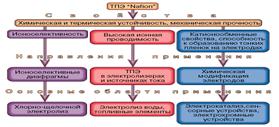
Рис. 2. Свойства и основные области применения ТПЭ "Nafion"
3.4 Электрохимическое получение хлора и гидроксида натрия
Хлор является важнейшим химическим продуктом, используемым для получения полимерных материалов, пестицидов, тканей. Его получают в настоящее время практически исключительно путем электролиза водного раствора хлорида натрия.
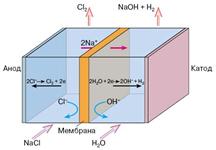
Рис. 3. Схема электрохимического синтеза хлора и гидроксида натрия с применением ТПЭ "Nafion"
Как показано на схеме процесса (рис. 3), на катоде (обычно сделанном из стали) происходит выделение водорода и образование гидроксильных ионов, дающих с находящимися в растворе ионами натрия гидроксид натрия. На аноде хлоридные анионы окисляются до молекулярного хлора. Этот процесс катализируется материалом анода, поверхность которого покрыта смесью оксидов титана и рутения (IV). При отсутствии разделительной диафрагмы гидроксильные ионы могут попадать из катодного пространства в анодное и взаимодействовать с хлором:
Cl2 + 2OH – → ClO – + Cl – + H2O
Кроме того, гипохлорит-ионы могут далее окисляться по реакции
6ClO – + 3H2O → 2ClO3 – + 4Cl – + 6H + + 1,5O2 + 6e –
Оба приведённых побочных процесса приводят к загрязнению щёлочи хлоратом натрия и появлению примеси кислорода в хлоре, резкому уменьшению выхода по току (показатель, характеризующий эффективность электрохимического процесса). Таким образом, присутствие разделительной мембраны, предотвращающей смешивание продуктов анодной и катодной реакций, является необходимым условием эффективного ведения процесса в целом. Мембрана должна соответствовать следующим требованиям:
— хорошо пропускать ионы Na +, но быть непроницаемой для ионов Cl – и OH — быть химически стабильной в высокоагрессивной среде (щелочной раствор хлорида натрия 6 моль/л при температуре 80–95&ddeg;С) в течение длительного времени;— иметь высокую электрическую проводимость; — быть механически прочной.
Эти требования были выполнены в полной мере только после появления мембран "Nafion", установки, на основе которых занимают в настоящее время, лидирующее положение в области хлорно-щелочного электролиза.
3.5 Кислородно-водородные генераторы и топливные элементы
Появление фторуглеродных катионообменных мембран произвело настоящую революцию в таких областях, как электролиз воды для получения водорода и кислорода и преобразование химической энергии в электрическую с помощью топливных элементов. Обе области науки и техники взаимосвязаны и являются необходимыми компонентами так называемой водородной энергетики. Суть последней состоит в преимущественном использовании водорода как экологически чистого и экономически выгодного энергоносителя. Действительно, водород может быть получен с помощью электролиза воды — принципиально экологически чистого процесса. Наиболее выгодно делать это в периоды наименьшей внешней загрузки электростанций. Далее, по существующим подсчётам, транспортировка водорода по системе трубопроводов обойдётся в пять раз дешевле передачи электрической энергии по высоковольтным линиям. У конечного потребителя водород может быть использован непосредственно как экологически чистый химический реагент (топливо, восстановитель) или для получения электрической энергии в топливных элементах. Использование водорода как энергоносителя поможет, таким образом, уменьшить расход углеводородного топлива и приведёт к уменьшению выбросов углекислого газа в атмосферу. Однако для реального внедрения концепции водородной энергетики необходимо решить несколько проблем, одной из которых является повышение эффективности электрохимического получения водорода и обратного преобразования химической энергии в электрическую. Как было отмечено, большую роль здесь сыграло появление мембраны "Nafion", которая в рассматриваемых системах является не только ион-селективной диафрагмой, но и действительно твёрдым полимерным электролитом. Принцип работы твёрдополимерного электролизёра может быть пояснён с помощью рис. 4.
