Коррозионные свойства титана и его сплавов
К третьей группе легирующих элементов, имеющих общие черты влияния на коррозионную стойкость титана, относятся Al, Sn, О, N, С. Установлено, что добавки алюминия снижают коррозионную стойкость титана в активном и пассивном состояниях. В нейтральных средах алюминий (до 5% Al) хотя и оказывает отрицательное влияние, но оно невелико. Понижение коррозионной стойкости при легировании алюминием связа
но с облегчением анодного и катодного процессов вследствие изменения химической природы пассивных пленок.
К четвертой группе легирующих элементов, однотипно влияющих на коррозионную стойкость титана, относятся металлы с низким сопротивлением катодному процессу. По возрастанию эффективности воздействия на титан эти элементы располагаются в следующий ряд: Си, W, Мо, Ni, Re, Ru, Pd, Pt.
Доказано, что введение в титановые сплавы таких элементов, как молибден, ниобий, цирконий, тантал не лимитируется по количеству. Они повышают коррозионную стойкость, способствуют увеличению прочности.
Электрохимическая коррозия под действием внутренних макро- и микрогальванических пар
Раньше электрохимическую коррозию называли гальванической коррозией, так как разрушение металла происходит под действием возникающих гальванических пар.
Рассмотрим различные случаи возникновения коррозионных гальванических пар.
1. Контакт с электролитом двух разных металлов в случае сочетания в одном узле или детали металлов различной активности в данной среде, или в случае применения сплава эвтектического типа из двух металлов разной активности.
2. Контакт металла и его соединения, обладающего металлообразными или полупроводниковыми свойствами. В любом случае свободный металл имеет отрицательный электрический заряд, а соединение — положительный заряд, так как в нем часть электронов проводимости связана. Это также справедливо и для интерметаллидов.
3. Различные концентрации электролитов или воздуха, растворенного в жидком электролите.
4. Различный уровень механических напряжений в одной и той же детали.
Рассмотрим более подробнее последний случай возникновения коррозионной гальванической пары. Коррозионные пары могут возникать при действии внешних или внутренних механических напряжений (остаточных напряжений, например при сварке). Если пластинку стали, дюраля или титанового сплава согнуть и в напряженном состоянии погрузить в коррозионную среду, то на растянутом слое (внешний) через относительно короткое время возникнут трещины (рис. 1), а внутренний сжатый слой будет оставаться без изменений. Растягивающие усилия особенно опасны, так как в этом случае металл повышает свою активность.
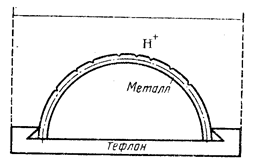
Рисунок 1 - Коррозия пластинки в напряженном состоянии
Если согнутую упруго пластинку (см. рис. 1) термически обработать и упругие деформации перейдут в пластические (явление релаксации), то разности потенциалов не возникает. Таким образом, при изготовлении деталей и узлов машин для снятия остаточных напряжений всегда следует термически обрабатывать изделия, если эти изделия предназначены для работы в сильно коррелирующих средах.
С этой целью в ИПСМ РАН при изготовлении тонких листов СМК - сплава ВТ6, полученных изотермической прокаткой, для более полного снятия остаточных напряжений и формирования зеренной структуры применяется крип-отжиг, который заключается в следующем: листы укладываются стопой между плоскими бойками и прижимаются под давлением 3-5 МПа при температуре 550 ˚С. После 20 мин выдержки нагрев выключается, и пакет остывает вместе со штамповым блоком в течение 12 часов.
Особенности взаимодействия титана с воздухом.
Воздух, представляющий собой смесь различных газов, является сложной газовой фазой, воздействие которой на титан может быть весьма многообразным. При этом взаимодействие титана с кислородом воздуха отличается от взаимодействия титана с чистым кислородом, так как на это взаимодействие оказывает влияние азот и другие составные части воздуха. Вместе с тем следует иметь в виду, что при всей сложности газовой фазы (воздуха) воздействие ее на титан следует рассматривать прежде всего как реакцию взаимодействия с ним самой активной и довольно значительной по количеству составляющей – кислорода.
Взаимодействие титана с кислородом.
При взаимодействии титана с кислородом происходит образование различных фаз химических соединений и твердых растворов.
При достаточно низких температурах взаимодействие титана с кислородом ограничивается адсорбцией. Начальная теплота адсорбции кислорода на титане при 25ОС составляет 989 кДж/моль; начальный коэффициент прилипания равен 1;0,8 и 0,67 при температурах -196; 25 и 300ОС соответственно. При дальнейшем взаимодействии на поверхности титана образуется оксидная плёнка.
В соответствии с термодинамическими расчетами оксидная пленка на титане должна состоять из слоев оксидов в последовательности:
Ti6O®Ti3O®Ti2O®Ti3O2®TiO®Ti13O5®TiO2
В действительности при окислении титана при температурах ниже 300OС оксидные слои состоят в основном из Ti3O5, при окислении в интервале температур 400-800OС образуется преимущественно рутил TiO2, а при температурах выше 800OС обнаружены оксиды TiO и Ti2O3. Согласно работе, окисление титана на воздухе и в кислороде до температур £ 600-650°С сопровождается образованием на образцах тонких оксидных пленок толщиной »0,1 мкм. Долей кислорода, растворенного в металлической основе при температурах ниже 450-500°С, по-видимому, можно пренебречь.
В работе [5] взаимодействие титана с кислородом описано следующим образом. Через возникающую на первых стадиях процесса пленку двуокиси титана TiO2 осуществляется диффузия кислорода к границе раздела пленка-металл, где происходит химическая реакция и дальнейший рост толщины пленки. Слой низших окислов титана, который должен присутствовать между слоем двуокиси и металлом, оказывается очень тонким и обычно не влияет на характер окисления. Скорость диффузии ионов титана через пленку по сравнению со скоростью диффузии титана очень мала. Однако при повышении температуры диффузия титана несколько увеличивается.
При небольшой продолжительности процесса, когда толщина пленки еще невелика, количество поступающего через пленку кислорода оказывается достаточным для окисления всего титана до двуокиси его. Вместе с тем по мере увеличения толщины пленки количество поступающего в зону кислорода уменьшается, а поступление титана остается постоянным, так как реакция происходит на границе раздела пленка-металл. В результате этого при достижении определенной толщины слоя окалины соотношение количеств титана и кислорода в зоне реакции становится таким, что между TiO2 и металлом образуется слой TiO. Появление его ослабляет сцепление окалины с металлом, которая под действием сжимающих напряжений деформируется и отслаивается, обнажая поверхность металла и обеспечивая скачкообразное увеличение скорости окисления. Однако возросшее поступление кислорода при отслаивании окалины приводит к окислению TiO до TiO2 и описанный выше процесс повторяется.
