Свойства азота
В ряду –N – P – As – Sb – Bi увеличиваются размеры атомов, ослабляется притяжение валентных электронов к ядру, ослабляются неметаллические свойства, возрастают металлические свойства, ЭО уменьшается. N, P - типичные неметаллы
As, Sb - проявляют неметаллические и металлические свойства
Bi - типичный металл
P, As и Bi существуют в твердом состоянии в нескольких модификациях.
1.
Основной характер оксидов R2O5 увеличивается, а кислотный – ослабевает с увеличением порядкового номера.
2. Гидроксиды всех элементов в пятивалентном состоянии имеют кислотный характер.
3. Основной характер гидроксидов R(OH)3 увеличивается, а кислотный – ослабевает с увеличением порядкового номера.
RO33- + 3H+ « R(OH)3 « R3+ + 3OH- (R – элемент)
4. As, Sb, и Bi плохо растворимы в воде.
5. Восстановительные свойства водородных соединений RH3 усиливаются, а устойчивость уменьшается с увеличением порядкого номера.
Эти элементы имеют 5 валентных электронов на наружном слое атома. Однако способность к присоединению электронов у них выражена значительно слабее, чем у элементов 7 и 6 группы [12,14].
Свойства азота. Изотопы, атом, молекула
Строение ядра и электронных оболочек. В природе существуют два стабильных изотопа азота: с массовым числом 14 (![]() содержит 7 протонов и 7 нейтронов) и с массовым числом 15 (
содержит 7 протонов и 7 нейтронов) и с массовым числом 15 (![]() содержит 7 протонов и 8 нейтронов). Их соотношение составляет 99,635:0,365, поэтому атомная масса азота равна 14,008. Нестабильные изотопы азота 12N, 13N, 16N, 17N получены искусственно. Схематически электронное строение атома
содержит 7 протонов и 8 нейтронов). Их соотношение составляет 99,635:0,365, поэтому атомная масса азота равна 14,008. Нестабильные изотопы азота 12N, 13N, 16N, 17N получены искусственно. Схематически электронное строение атома ![]() азота таково: 1sІ2sІ2p№x2p№y2p№z. Следовательно, на внешней (второй) электронной оболочке находится 5 электронов, которые могут участвовать в образовании химических связей; орбитали азота могут также принимать электроны, т.е. возможно образование соединений со степенью окисления от (–III) до (V), и они известны. Особенно большой интерес представляли данные о содержании изотопа азота-15, так как именно этот изотоп в 1997 г. обнаружили в комете Хейла-Боппа, которая тогда пролетала мимо Солнца и была хорошо видна на небе невооруженным глазом. Как оказалось, соотношение изотопов азота-15 и азота-14 у этих комет почти одинаковое: один атом азота-15 приходится на 140 атомов азота-14 (погрешность измерений составляет +/-30 атомов). Это почти вдвое больше, чем на Земле (272 атома азота-14 на один атом азота-15). Кроме того, это сильно отличается от того же соотношения изотопов в комете Хейла-Боппа, полученного с помощью измерений радиоспектров молекул CN и HCN. Астрономы объясняют это тем, что изотоп азота-15 входит не только в молекулы HCN и CN, но и в молекулы каких-то других веществ, имеющихся в частицах пыли, вмерзших в ядро кометы.
азота таково: 1sІ2sІ2p№x2p№y2p№z. Следовательно, на внешней (второй) электронной оболочке находится 5 электронов, которые могут участвовать в образовании химических связей; орбитали азота могут также принимать электроны, т.е. возможно образование соединений со степенью окисления от (–III) до (V), и они известны. Особенно большой интерес представляли данные о содержании изотопа азота-15, так как именно этот изотоп в 1997 г. обнаружили в комете Хейла-Боппа, которая тогда пролетала мимо Солнца и была хорошо видна на небе невооруженным глазом. Как оказалось, соотношение изотопов азота-15 и азота-14 у этих комет почти одинаковое: один атом азота-15 приходится на 140 атомов азота-14 (погрешность измерений составляет +/-30 атомов). Это почти вдвое больше, чем на Земле (272 атома азота-14 на один атом азота-15). Кроме того, это сильно отличается от того же соотношения изотопов в комете Хейла-Боппа, полученного с помощью измерений радиоспектров молекул CN и HCN. Астрономы объясняют это тем, что изотоп азота-15 входит не только в молекулы HCN и CN, но и в молекулы каких-то других веществ, имеющихся в частицах пыли, вмерзших в ядро кометы.
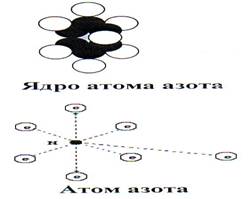
Структура атома азота близка по форме к структуре ядра атома углерода. Поскольку большинство ядер атомов азота имеют семь протонов и семь нейтронов, то это большинство имеет плоские ядра, показанные на рис. 1, а. Схема атома азота, имеющего такое ядро, показана на рис. 1, б. Атом азота имеет лишь один активный (валентный) электрон. Именно эта особенность создаёт условия для формирования молекулы из двух атомов со столь большой энергией связи, что химики придумали для неё название тройной связи [2]. Нет, связь у молекулы азота одна, но с большой энергией связи. Жаль, что спектр атома азота смешан со спектром его молекулы. Приводимая в справочниках по спектроскопии энергия ионизации атома азота, равная 14,534 eV, скорее всего, является энергией диссоциации молекулы азота, а не энергией ионизации его атома. Это достаточно большая энергия связи. Представим процесс перехода шести кольцевых электронов атома азота на нижние энергетические уровни. Его особенность заключается в том, что эти электроны переходят на нижние энергетические уровни одновременно, излучая при этом фотоны, размеры, которых на несколько порядков больше размера атома азота. Когда в этот процесс вовлекается вся совокупность атомов азота вещества, в которое он входит, и когда в него вовлекаются атомы углерода и кислорода, которые также имеют кольцевую совокупность электронов, то суммарное количество излученных фотонов сразу увеличивает объём, занимаемый ими в пространстве, что и формирует явление взрыва. Конечно, существующее представление о том, что взрыв – расширение газов – глубоко ошибочно. Давление формируют одновременно излучаемые фотоны благодаря тому, что их размеры на 5-7 порядков больше размеров атомов. Из этого сразу вытекают неизвестные специалистам требования к взрывчатым веществам и ракетному топливу и методы их реализации, но мы не будем развивать эту тему по известным причинам.
Из определений плотности газа установлено, что молекула азота двухатомна, т.е. молекулярная формула азота имеет вид N≡N (или N2). У двух атомов азота три внешних 2p-электрона каждого атома образуют тройную связь:N:::N:, формируя электронные пары. Измеренное межатомное расстояние N–N равно 1,095 Е. Как и в случае с водородом, существуют молекулы азота с различным спином ядра – симметричные и антисимметричные. При обычной температуре соотношение симметричной и антисимметричной форм равно 2:1. В твердом состоянии известны две модификации азота: α – кубическая и β – гексагональная с температурой перехода α в β–237,39° С. Модификация β плавится при –209,96° С и кипит при –195,78° C при 1 атм.
Энергия диссоциации моля (28,016 г или 6,023·10Іі молекул) молекулярного азота на атомы (N2 2N) равна примерно –225 ккал. Поэтому атомарный азот может образовываться при тихом электрическом разряде и химически более активен, чем молекулярный азот.
Энергетическая схема заполнения молекулярных орбиталей в молекуле N2 показывает, что электронами в ней заполнены только связывающие s- и p-орбитали. Молекула азота немагнитна (диамагнитна).Молекула N2 является наиболее прочной среди гомоатомных молекул типа A2 . Энергия диссоциации N2 на два атома азота (Eд) составляет 941,6 кДж/моль. Валентная оболочка двухатомных молекул (N2 , CO, O2 , NO, F2) состоит из трех связывающих и трех разрыхляющих молекулярных орбиталей (МО). На трех связывающих МО молекулы N2 находятся шесть 2p-электронов двух атомов азота, причем 4p-электрона размещаются на двух p-орбиталях (1pu) и 2p-электрона - на верхней s-орбитали (3sg):
На этой диаграмме молекулярных орбиталей цифры обозначают номер орбитали данного типа, pu и sg - связывающие p- и s-, а и - разрыхляющие МО. Таким образом, высшая занятая МО из трех образующих тройную связь, за счет которой молекула N2 проявляет донорные свойства, является s-МО в отличие от молекулы С2Н2 , в которой высшие занятые МО - орбитали p-типа.
Энергия отрыва электрона (потенциал ионизации I ) с 3sg-орбитали N2 очень высока, близка к потенциалу ионизации инертного газа аргона и намного выше потенциала ионизации ксенона и кислорода: = 15,6 эВ, IAr = 15,76 эВ, IXe = 12,1 эВ, = 12,1 эВ. Пары 2s-электронов, которые обычно изображают в виде точек на атомах азота (:NЇN:), вообще не участвуют во взаимодействии с акцепторами электронов, так как находятся на 2sg- и -МО, лежащих существенно ниже 1pu-МО, потенциал ионизации которой 17,1 эВ. Именно из-за слабых электронодонорных свойств N2 только очень сильные акцепторы в газовой фазе (H+, BF3) взаимодействуют с этой молекулой: , F3B(N2).
