Получение хлора методом электролиза повареной соли
![]() ,
,
или после преобразования:
![]() .
.
Учитывая, что число переноса катиона ![]() , получим:
, получим:
![]() .
.
На аноде выделяется height=41 src="images/referats/13731/image046.png">молей газообразного хлора. Если принебречь объемом
![]() и
и ![]() и подсасываемого к хлору воздуха, то количество молей влаги, уносимой с хлор-газом в виде паров, составит:
и подсасываемого к хлору воздуха, то количество молей влаги, уносимой с хлор-газом в виде паров, составит:
![]() ,
,
где ![]() - общее давление влажного газа;
- общее давление влажного газа;
![]() - парциальное давление паров воды в хлоре над анолитом.
- парциальное давление паров воды в хлоре над анолитом.
Моляльность анолита можно определить из выражения:
![]() или
или 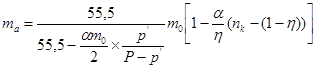 .
.
При ![]()
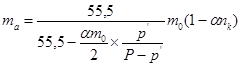 .
.
На катоде образуется ![]() молей гидроокиси натрия и выделяется
молей гидроокиси натрия и выделяется ![]() молей газообразного водорода, при этом на химическую реакцию расходуется
молей газообразного водорода, при этом на химическую реакцию расходуется ![]() молей воды. Количество воды, уносимой с водородом в виде паров воды, составит:
молей воды. Количество воды, уносимой с водородом в виде паров воды, составит:
![]() ,
,
где ![]() – парциальное давление паров воды в водороде над католитом.
– парциальное давление паров воды в водороде над католитом.
Содержание поваренной соли в католите определяется по разности между поступившим и разложившимся количествами:
![]() .
.
Содержание воды в католите составит:
![]() .
.
Моляльность католита (по ![]() ) составит:
) составит:
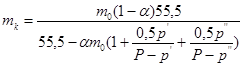 ,
,
А по ![]() :
:
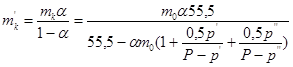 .
.
Суммарная мольяность католита по ![]() и
и ![]() :
:
![]() .
.
Степень изменения количества воды в электролите в процессе электролиза:
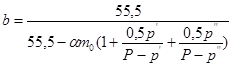 .
.
Чтобы перевести единицы концентрации из мольяльности в г/л (![]() ) можно воспользоваться выражением:
) можно воспользоваться выражением:
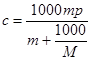 ,
,
где ![]() - моляльность раствора;
- моляльность раствора;
![]() - плотность раствора;
- плотность раствора;
![]() - молекулярный вес растворенной соли.
- молекулярный вес растворенной соли.
Моляльность католита по поваренной соли и каустической соде составит:
![]() ,
,
![]() .
.
Снижение парциального давления паров воды над электролитическими щелаками ![]() может быть приближенно принято равным сумме снижения парциального давления над соответствующими растворами гидроокиси натрия
может быть приближенно принято равным сумме снижения парциального давления над соответствующими растворами гидроокиси натрия ![]() .
.
![]() .
.
При таком подсчете парциальные давления паров воды над католитом мало отличаются от парциального давления над насыщенным раствором поваренной соли при той же температуре.
Если принять, что ![]() , то тогда получаем:
, то тогда получаем:
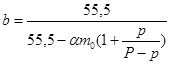 .
.
При парциальном давлении паров воды над электролитом выше 400–500 мм. рт. ст. унос паров воды резко возрастает. При парциальном давлении паров около 720 мм. рт. ст. теоретически с газами должно быть унесена вся вода из раствора. Поэтому при сильном повышении температуры электролиза происходит интенсивное испарение влаги, пересыщение раствора и выделения кристаллов соли, которые забивают поры диафрагмы и приводят к нарушению нормального процесса электролиза.
Материальный баланс элетролизера осложняется наличием примесей, например соды, щелочи и сульфатов, в мешающем электролизу растворе, протеканием процессов выделения на аноде кислорода и окисления графитовых анодов в образованием в основном двуокиси углерода, а также вторичных процессов растворения и гидролиза хлора в анолите и последующих реакций между растворенным хлором и ионами ![]() с образованием гипохлорита и хлората. Однако для практических целей приведенная выше приближенная схема расчета материального баланса дает достаточно точные результаты.
с образованием гипохлорита и хлората. Однако для практических целей приведенная выше приближенная схема расчета материального баланса дает достаточно точные результаты.
Образующийся в электролизере гипохлорит практически полностью восстанавливается на катоде с образованием исходного хлорида натрия. Количество хлората натрия, уходящего с катодными щелоками, не превышает обычно десятых долей процента от образовавшейся каустической соды. Поэтому в практических балансах электролизера эти процессы могут не учитываться. Расчет воды и образования двуокиси углерода за счет сгорания анодов в связи с выделением кислорода можно учесть приближенно, приняв, что снижение выхода по току связано лишь с разрядом ионов ![]() на анод.
на анод.
Расход воды на разложение составит ![]() , а количество двуокиси углерода, образовавшегося от сгорания анодов, равно
, а количество двуокиси углерода, образовавшегося от сгорания анодов, равно ![]() . При температуре 90–95 °С, поддерживаемой в современных электролизерах, потери воды на побочные процессы не превышает 0,5–1,0% общего расхода воды на химические процессы и испарение.
. При температуре 90–95 °С, поддерживаемой в современных электролизерах, потери воды на побочные процессы не превышает 0,5–1,0% общего расхода воды на химические процессы и испарение.
Заключение
В настоящее время едкая щёлочь и хлор вырабатываются тремя электрохимическими методами. Два из них – электролиз с твёрдым асбестовым или полимерным катодом (диафрагменный и мембранный методы производства), третий – электролиз с жидким ртутным катодом (ртутный метод производства). В ряду электрохимических методов производства самым лёгким и удобным способом является электролиз с ртутным катодом, но этот метод наносит значительный вред окружающей среде в результате испарения и утечек металлической ртути. Мембранный метод производства самый эффективный, наименее энергоемкий и наиболее экологичный, но и самый капризный, в частности, требует сырье более высокой чистоты.
